Нові публікації
Активація вродженого імунітету: виявлено важливу частину механізму
Останній перегляд: 02.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
Дослідники з Університету Луїзіани розшифрували складну взаємодію різних ферментів навколо вродженого імунного рецептора Toll-подібного рецептора 7 (TLR7), який відіграє важливу роль у захисті нашого організму від вірусів.
Toll-подібний рецептор 7 (TLR7), розташований на дендритних клітинах нашої імунної системи, відіграє вирішальну роль у нашому природному захисті від вірусів. TLR7 розпізнає одноланцюгову вірусну та іншу чужорідну РНК та активує вивільнення медіаторів запалення. Дисфункції цього рецептора також відіграють ключову роль в аутоімунних захворюваннях, що робить розуміння та, в ідеалі, модуляцію механізму активації TLR7 ще важливішим.
Дослідники під керівництвом професора Файта Горнунга та Марлен Беруті з Генетичного центру Мюнхена та кафедри біохімії в LMU змогли глибше зануритися в механізм активації комплексу. З попередніх досліджень було відомо, що складні молекули РНК повинні бути розрізані, щоб рецептор міг їх розпізнати.
Використовуючи низку технологій, від клітинної біології до кріоелектронної мікроскопії, дослідники LMU виявили, як одноланцюгова чужорідна РНК обробляється для виявлення TLR7. Їхня робота була опублікована в журналі Immunity.
Численні ферменти беруть участь у розпізнаванні чужорідної РНК
Протягом еволюції імунна система спеціалізувалася на розпізнаванні патогенів за їхнім генетичним матеріалом. Наприклад, вроджений імунний рецептор TLR7 стимулюється вірусною РНК. Ми можемо уявляти вірусну РНК як довгі ланцюги молекул, які занадто великі, щоб їх можна було розпізнати як ліганди для TLR7. Саме тут на допомогу приходять нуклеази — молекулярні ріжучі інструменти, які розрізають «ланцюг РНК» на дрібні шматочки.
Ендонуклеази розрізають молекули РНК посередині, як ножиці, тоді як екзонуклеази розщеплюють ланцюг від одного кінця до іншого. Цей процес генерує різні фрагменти РНК, які тепер можуть зв'язуватися з двома різними кишенями на рецепторі TLR7. Тільки коли обидві кишені зв'язування на рецепторі зайняті цими фрагментами РНК, запускається сигнальний каскад, який активує клітину та запускає стан тривоги.
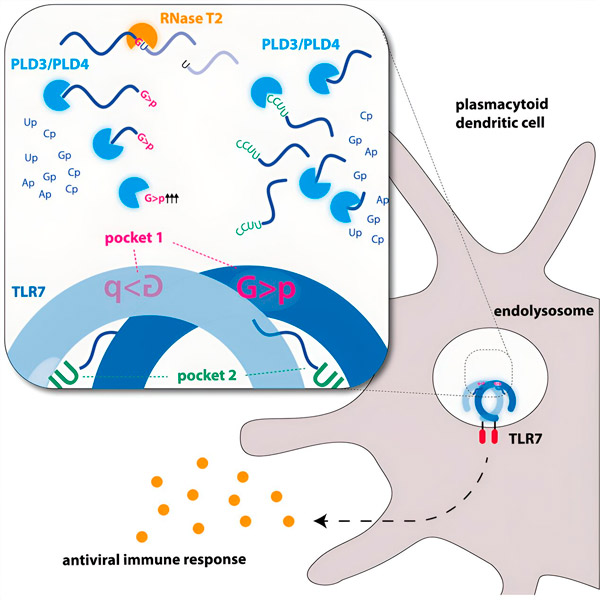
Графічне зображення. Джерело: Імунітет (2024). DOI: 10.1016/j.immuni.2024.04.010
Дослідники виявили, що для розпізнавання РНК TLR7 потрібна активність ендонуклеази РНКази T2, яка діє разом з екзонуклеазами PLD3 та PLD4 (фосфоліпаза D3 та D4). «Хоча було відомо, що ці ферменти можуть розщеплювати РНК, — каже Хорнунг, — тепер ми продемонстрували, що вони взаємодіють з TLR7 і тим самим його активують».
Балансування імунної системи
Дослідники також виявили, що екзонуклеази PLD відіграють подвійну роль в імунних клітинах. У випадку TLR7 вони мають прозапальний ефект, тоді як у випадку іншого рецептора TLR, TLR9, вони мають протизапальний ефект. «Ця подвійна роль екзонуклеаз PLD вказує на тонко скоординований баланс для контролю належних імунних реакцій», – пояснює Беруті.
«Одночасна стимуляція та пригнічення запалення цими ферментами може служити важливим захисним механізмом для запобігання дисфункціям у системі». Яку роль можуть відігравати інші ферменти в цьому сигнальному шляху та чи підходять залучені молекули як цільові структури для терапії, стане предметом подальших досліджень.
