Нові публікації
Ракові клітини миттєво активують вироблення енергії, коли ДНК стискається та пошкоджується
Останній перегляд: 03.08.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
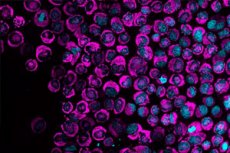
Згідно з дослідженням, опублікованим у журналі Nature Communications, ракові клітини миттєво активують енергетичну реакцію на фізичне стиснення. Цей сплеск енергії є першим задокументованим проявом захисного механізму, який допомагає клітинам відновлювати пошкоджену ДНК та виживати в обмежених умовах людського тіла.
Ці висновки допомагають пояснити, як ракові клітини виживають у складних механічних середовищах, таких як повзання крізь мікрооточення пухлини, проникнення крізь пористі кровоносні судини або подолання ударів у кровотоці. Відкриття цього механізму може призвести до нових стратегій «закріплення» ракових клітин до їх поширення.
Дослідники з Центру геномної регуляції (CRG) у Барселоні зробили це відкриття за допомогою спеціалізованого мікроскопа, здатного стискати живі клітини до розміру всього три мікрони – приблизно в тридцять разів меншого за діаметр людської волосини. Вони спостерігали, що протягом кількох секунд після стиснення мітохондрії в клітинах HeLa кидалися на поверхню ядра та починали закачувати додаткову кількість АТФ, молекулярного джерела енергії клітин.
«Це змушує нас переосмислити роль мітохондрій в організмі людини. Вони не просто статичні батареї, що живлять клітини, а радше розумні «рятівники», до яких можна звернутися в надзвичайній ситуації, коли клітина буквально доведена до межі своїх можливостей», — каже доктор Сара Сделчі, співавтор дослідження.
Мітохондрії утворювали таке щільне «світіння» навколо ядра, що ядро стискалося всередину. Це явище спостерігалося у 84 відсотках стиснутих ракових клітин HeLa, порівняно з майже нульовим показником у плаваючих, нестиснених клітинах. Дослідники назвали ці структури NAM (nucleus-associated mitochondrias – мітохондрії, пов'язані з ядром).
Щоб з'ясувати, що роблять NAM, дослідники використали флуоресцентний датчик, який засвічується, коли АТФ потрапляє в ядро. Сигнал збільшувався приблизно на 60% лише через три секунди після стиснення клітин.
«Це чітка ознака того, що клітини адаптуються до стресу та переналаштовують свій метаболізм», – пояснює доктор Фабіо Пеццано, перший співавтор дослідження.
Подальші експерименти показали, чому це підвищення енергії має значення. Механічне стиснення напружує ДНК, розриваючи нитки та сплутуючи геном. Клітинам потрібні АТФ-залежні репараційні комплекси, щоб послабити структуру ДНК та дістатися до пошкодження. Стиснуті клітини, які отримали додатковий АТФ, відновлювали свою ДНК протягом кількох годин, тоді як клітини без додаткового АТФ переставали нормально ділитися.
Щоб підтвердити значення цього механізму в розвитку захворювання, дослідники також дослідили біопсії пухлин молочної залози від 17 пацієнтів. Ореоли NAM спостерігалися у 5,4% ядер на інвазивному краї пухлини порівняно з 1,8% у щільному ядрі — різниця втричі.
«Те, що ми виявили цю ознаку в тканинах пацієнта, підтвердило її значення поза межами лабораторії», – пояснює доктор Рітобрата (Ріто) Гхоуз, перший співавтор дослідження.
Дослідники також змогли вивчити клітинні механізми, що забезпечують мітохондріальний «потоп». Актинові філаменти — ті ж білкові нитки, що дозволяють м'язам скорочуватися — утворюють кільце навколо ядра, а ендоплазматичний ретикулум стягує сітчасту «пастку» разом. Дослідження показало, що таке комбіноване розташування фізично утримує NAM на місці, утворюючи «гало». Коли дослідники обробили клітини латрункуліном А, препаратом, який порушує актин, утворення NAM зникло, а рівень АТФ різко знизився.
Якщо метастатичні клітини залежать від сплесків АТФ, пов'язаних з NAM, то препарати, що порушують каркас, можуть зробити пухлини менш інвазивними, не отруюючи самі мітохондрії та не впливаючи на здорові тканини.
«Механічні стресові реакції — це погано вивчена вразливість ракових клітин, яка може відкрити нові терапевтичні підходи», — сказала доктор Верена Рупрехт, співавтор дослідження.
Хоча дослідження зосереджувалося на ракових клітинах, автори зазначають, що це, ймовірно, універсальне явище в біології. Імунні клітини, що проходять через лімфатичні вузли, процеси росту нейронів та ембріональні клітини під час морфогенезу – всі вони зазнають подібного фізичного стресу.
«Там, де клітини перебувають під тиском, сплеск енергії до ядра, ймовірно, захищає цілісність геному», – підсумовує доктор Сделчі. «Це абсолютно новий рівень регуляції в клітинній біології, що являє собою фундаментальний зсув у нашому розумінні того, як клітини переживають фізичний стрес».
