Нові публікації
Штучний інтелект виявляє рак простати на ранній стадії, пропущений патологоанатомами
Останній перегляд: 23.08.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
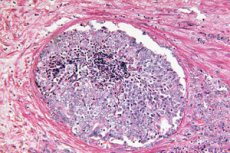
У дослідженні «Наукові звіти» демонструють, що штучний інтелект може розпізнавати приховані морфологічні ознаки пухлини в біоптатах простати, які раніше патологоанатом вважав доброякісними. Модель глибокого навчання, навчена з використанням слабо контрольованого підходу, передбачила, у яких чоловіків з підвищеним рівнем ПСА розвинеться клінічно значущий рак простати (ISUP > 1) протягом наступних 30 місяців, а у яких рак не буде протягом щонайменше 8 років. Це відкриває шлях до ранньої стратифікації ризику одразу після початкової «чистої» біопсії та може допомогти вирішити, кому дійсно потрібні повторні інвазивні процедури та посилений нагляд.
Передумови дослідження
Первинна голкова біопсія простати часто дає хибнонегативні результати: значна частина клінічно значущого раку залишається «поза екраном», особливо при традиційній систематичній ТРУЗІ-біопсії. Впровадження МРТ-контролю збільшило частку виявлення клінічно значущого раку та зменшило кількість непотрібних повторних процедур, але навіть за сучасних стратегій деякі агресивні пухлини залишаються невиявленими. Клінічна дилема залишається незмінною: кого слід спостерігати після «чистої» біопсії, а кого слід направити на ранню повторну біопсію, щоб не затримувати діагностику та не перевантажувати пацієнтів інвазивними втручаннями.
Біологічною основою вирішення цієї проблеми є феномен TINT (пухлинно-інструктована/вказівна на нормальну тканину): пухлина «переналаштовує» навколишні, здавалося б, нормальні тканини органу, залишаючи в них слабкі, але систематичні сліди – від ремоделювання строми та гіпоксії до метаболічних зрушень. Ці зміни були описані в експериментальних моделях та у пацієнтів з раком простати та корелюють з агресивністю пухлини, що робить «нормальну» тканину потенційним джерелом діагностичних сигналів, навіть якщо в ядрі біопсії немає очевидних ракових залоз.
Методи цифрової патології та глибокого навчання спрямовані на вилучення таких «тонких» польових ознак зі стандартних зрізів гемоглобіну та еозинофілії (Г&Е). На відміну від класичної морфології, яка зосереджена на очевидних структурах пухлини, алгоритми можуть фіксувати розподілені закономірності в стромі та епітелії, пов'язані з наявністю пухлини в іншій частині органу. Це відкриває шлях до стратифікації ризику одразу після негативної біопсії: високий «оцінка» за шкалою скляного скляного штриха свідчить про доцільність ранньої повторної біопсії або наведення за допомогою МРТ, низький – на підтримку більш щадного спостереження.
Це ідея, що лежить в основі нового дослідження, опублікованого в Scientific Reports: автори перевірили, чи може штучний інтелект передбачити клінічно значущий рак простати протягом наступних 30 місяців на основі морфологічних ознак біоптатів TINT. Робота базується на раніше представленому препринті та формує прикладну основу для впровадження «польових» цифрових біомаркерів у маршрутизацію пацієнтів після початкової «чистої» біопсії.
Як це було зроблено: дизайн, дані, алгоритм
Автори ретроспективно зібрали когорту з 232 чоловіків з підвищеним рівнем ПСА та початковим висновком «доброякісний» за даними голкової біопсії (після технічного контролю до остаточного аналізу було включено 213 пацієнтів та 587 зрізів; біопсії 1997-2016, Умео, Швеція). Кожному пацієнту було зіставлено «дзеркальну» пару за віком, роком постановки діагнозу та рівнем ПСА: у половини рак простати був діагностований пізніше (≤30 місяців), інша половина залишалася без раку протягом щонайменше 8 років. Препарати Г&Е були оцифровані (20×), нарізані на плитки розміром 256×256 пікселів та передані до CLAM (Clustering-constrained Attention Multiple-Instance Learning) – сучасної слабо контрольованої схеми, де відома лише доля пацієнта, а не маркування кожного пікселя. Ознаки були вилучені за допомогою ResNet18, попередньо навченого на 57 наборах гістопатологічних даних. Кінцева точка є бінарною: низький ризик (доброякісний/ISUP1) проти високого ризику (ISUP2-5).
Точність прогнозування
У незалежному тестуванні модель досягла AUC 0,81 на всіх препаратах та AUC 0,82 на рівні пацієнта. При порозі, що забезпечував прийнятний баланс, чутливість становила 0,92 з рівнем хибнопозитивних результатів 0,32 (на рівні пацієнта). Іншими словами, серед людей, чия початкова біопсія була «невдалою», штучний інтелект правильно позначив переважну більшість тих, у кого невдовзі було підтверджено клінічно значущий рак, хоча й ціною деяких хибних тривог. Для клініки це сигнал: «доброякісна» відповідь на біопсію ≠ нульовий ризик, і її можна кількісно стратифікаціїти за допомогою цифрового скла.
Що саме «помічає» ШІ у «нормальній» тканині?
Інтерпретація за допомогою UMAP та карт уваги показала, що зміни строми є найбільш інформативними:
- Більше колагену в стромі (ущільнення матриксу, «фіброз»);
- Менша кількість гладком'язових клітин навколо залоз;
- Менш поширеними є ледь помітні сигнали в залозистому епітелії, ймовірно, нижче доступної роздільної здатності даунсемплінгу.
Цей патерн відповідає концепції TINT (пухлинно-інструктована/вказівна нормальна тканина): навіть «норма» в органі, де прихована пухлина, переналаштовується під її впливом і відрізняється від «норми» в органі без пухлини. Рак — це не лише вогнище, а й поле, і ШІ вчиться зчитувати ефект поля.
Як цей підхід корисний на практиці – можливі сценарії
- Повторна біопсія на основі ризику: високий показник штучного інтелекту на «чистому» склі – аргумент на користь ранньої повторної біопсії або наведення за допомогою МРТ замість очікування.
- Персоналізація моніторингу: Низька швидкість врівноважує тривожність після «прикордонної» МРТ та дозволяє модифікувати інтенсивність моніторингу.
- Навчання шаблону TINT: карти уваги та інтерактивні накладання допомагають патологоанатомам бачити ледь помітні поля навколо раку, покращуючи узгодженість звітів.
Важливо розуміти обмеження
Це єдиний центр на півночі Швеції (переважно європеоїдне населення), дизайн є ретроспективним, базові біопсії проводилися без наведення МРТ (систематичні ТРУЗІ-біопсії), а маркери є майбутніми результатами, а не «прихованою пухлиною на одному предметному склі». Зовнішньої валідації в незалежних центрах/сканерах поки що немає, як і проспективного дослідження впливу алгоритму на клінічні рішення та результати. Рівень хибнопозитивних результатів залишається значним – модель не замінює лікаря, але додає ймовірнісний шар для спільного прийняття рішень.
Що далі: Дорожня карта впровадження
- Багатоцентрова зовнішня валідація (різні сканери, протоколи, етнічні групи).
- Проспективні дослідження рішень: чи змінює шкала штучного інтелекту траєкторію розвитку пацієнта (час до постановки діагнозу, кількість непотрібних повторних біопсій, гіпер/недостатній діагноз).
- Інтеграція з МРТ та клінікою: комбіновані моделі (PSA, MRI PIRADS, клінічні фактори + оцінка TINT згідно з шкалою H&E).
- Технічні кроки: стандартизація цифровізації, контроль дрейфу даних, пояснимість (накладання уваги на рутину).
Джерело: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C. та ін. Виявлення пухлини, що вказує на морфологічні зміни в доброякісних біоптатах простати за допомогою штучного інтелекту. Наукові звіти (Nature Portfolio), опубліковані 21 серпня 2025 року. DOI: https://doi.org/10.1038/s41598-025-15105-6
