Нові публікації
TIVDAK®, схвалений FDA: Направлення на тканинний фактор при раку шийки матки
Останній перегляд: 02.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
29 квітня 2024 року Управління з контролю за продуктами харчування та лікарськими засобами США (FDA) надало повне схвалення препарату TIVDAK® (тисотумаб ведотин) компанії Seagen Inc., що діє на тканинний фактор (ТФ), для лікування пацієнтів з рецидивуючим або метастатичним раком шийки матки, який прогресував під час або після хіміотерапії. Це є значним проривом у терапії раку шийки матки, що підкреслює потенціал кон'югатів антитіл та лікарських засобів (ADC) в онкології.
Механізм дії препарату ТІВДАК
Tivdak – це ADC, що націлений на TF, шляхом поєднання моноклонального антитіла проти TF тизотумабу від Genmab з технологією ADC від Seagen, розробленою для впливу на антигени TF на ракових клітинах та доставки цитотоксичного компонента MMAE безпосередньо до ракових клітин.
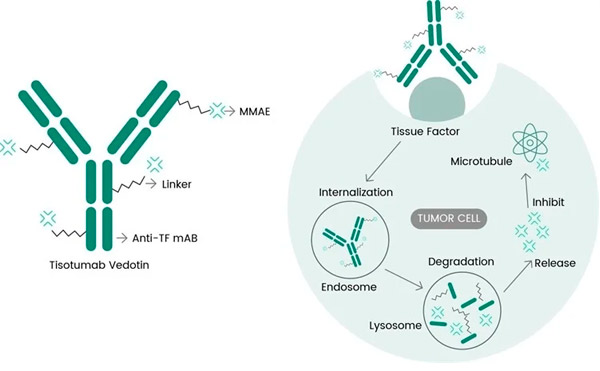
Молекулярний механізм дії тисотумабу ведотину ( https://doi.org/10.3390/ijms23073559 )
TF: Ідеальна ціль для розробки АЦП
Відомо, що ТФ бере участь у пухлинній сигналізації та ангіогенезі, і його надмірна експресія спостерігається у переважної більшості пацієнтів з раком шийки матки та багатьма іншими солідними пухлинами. Його здатність швидко засвоюватися після зв'язування з антитілами та мінімальний вплив на нормальне згортання крові ще більше підвищують його придатність для цільової терапії раку.
