Виявлено білок, відповідальний за генетичне запальне захворювання
Останній перегляд: 14.06.2024

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
Команда дослідників на чолі з доктором Хіроцугу Ода з Кластера передового досвіду дослідження старіння CECAD Кельнського університету виявила роль, яку певний білковий комплекс відіграє в деяких формах імунної дисрегуляції. Цей результат може призвести до розробки нових терапевтичних підходів, спрямованих на зменшення автоінфляції та «відновлення» імунної системи пацієнтів, які страждають від генетичної дисфункції цього білкового комплексу.
Дослідження «Biallelic human SHARPIN disfunction induces autoflammation and immunodeficiency» було опубліковано в Nature Immunology.
Лінійний комплекс збирання убіквітину (LUBAC), що складається з білків HOIP, HOIL-1 і SHARPIN, давно визнано своєю критичною роллю в підтримці імунного гомеостазу. Попередні дослідження на мишах показали серйозні наслідки втрати SHARPIN, що призвело до важкого дерматиту внаслідок надмірної загибелі клітин шкіри. Однак конкретні наслідки дефіциту SHARPIN для здоров’я людини поки що залишаються нез’ясованими.
Дослідницька група вперше повідомляє про двох людей із дефіцитом SHARPIN, які виявляють симптоми аутоінфляції та імунодефіциту, але неочікувано не виявляють дерматологічних проблем, як у мишей.
Після подальшого дослідження було виявлено, що у цих осіб порушена канонічна відповідь NF-κB, шлях, важливий для імунної відповіді. Вони також мали підвищену чутливість до загибелі клітин, спричиненої членами надродини фактора некрозу пухлин (TNF). Лікування одного з пацієнтів із дефіцитом SHARPIN анти-TNF-терапією, яка специфічно інгібує TNF-індуковану загибель клітин, призвело до повного зникнення аутоінфляції на клітинному рівні та клінічних проявів.
Дослідження показують, що надмірна та неконтрольована смерть клітин відіграє вирішальну роль у генетичних запальних захворюваннях людини. Команда Оди додала дефіцит SHARPIN як нового члена групи генетичних запальних захворювань людини, які вони пропонують назвати «вроджені помилки смерті клітин».
Захист від імунної дисрегуляції Дослідження було розпочато в лабораторії доктора Дена Кастнера в Національному інституті здоров’я (NIH) у Сполучених Штатах. Вченим вдалося спостерігати за одним пацієнтом із незрозумілими епізодами лихоманки, артриту, коліту та імунодефіциту в дитинстві.
Отримавши інформовану згоду, вони провели секвенування екзома на пацієнті та його родині та виявили, що пацієнт мав руйнівний генетичний варіант у гені SHARPIN, що призводить до невизначуваних рівнів білка SHARPIN. Вони також виявили, що клітини пацієнтів демонструють підвищену схильність до загибелі як у культивованих клітинах, так і в біопсіях пацієнтів.
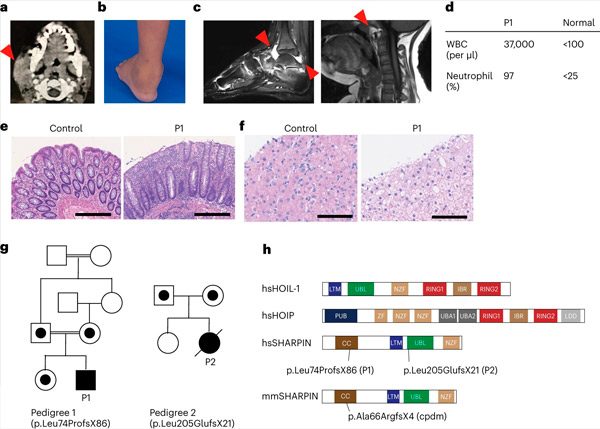
Дефіцит SHARPIN у людей викликає аутозапалення та глікогеноз печінки. Джерело: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Команда також виявила, що розвиток лімфоїдних зародкових центрів – спеціалізованих мікроструктур в аденоїдах, які мають вирішальне значення для дозрівання В-клітин нашої імунної системи і, отже, вироблення антитіл, – значно зменшився через збільшення загибелі В-клітин. Ці результати пояснюють імунодефіцит у пацієнтів і підкреслюють важливу роль LUBAC у підтримці імунного гомеостазу у людей.
«Наше дослідження підкреслює критичну важливість LUBAC для захисту від імунної дисрегуляції. З’ясовуючи молекулярні механізми, що лежать в основі дефіциту LUBAC, ми прокладаємо шлях для нових терапевтичних стратегій, спрямованих на відновлення імунного гомеостазу», – сказав Ода, провідний автор дослідження.
Він додав: «Один із пацієнтів із дефіцитом SHARPIN залежав від інвалідного візка багато років, перш ніж ми вперше його побачили. Його щиколотки боліли, і ходити було надто боляче. Генетична діагностика дозволила нам визначити правильний молекулярний шлях, що лежить в основі його захворювань."
Відтоді як пацієнт почав отримувати терапію проти TNF, у нього майже сім років не було симптомів. «Як клініцист і вчений, я радий мати можливість позитивно вплинути на життя одного пацієнта завдяки нашим дослідженням», — підсумував Ода.
