Нові публікації
Новий пристрій покращує генерацію стовбурових клітин для терапії Альцгеймера
Останній перегляд: 02.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.

Шведські дослідники стверджують, що вони вдосконалили техніку перетворення звичайних клітин шкіри на нейронні стовбурові клітини, що, за їхніми словами, наближає їх до доступної персоналізованої клітинної терапії хвороби Альцгеймера таПаркінсона.
Використовуючи спеціально розроблений мікрофлюїдний пристрій, дослідницька група розробила безпрецедентний та прискорений підхід до перепрограмування клітин шкіри людини в індуковані плюрипотентні стовбурові клітини (iPSC) з подальшим перетворенням їх на нейронні стовбурові клітини.
Перший автор дослідження, Саум'я Джайн, каже, що платформа може покращити та знизити вартість клітинної терапії, зробивши клітини більш сумісними та прийнятними організмом пацієнта. Дослідження було опубліковано в журналі Advanced Science вченими з Королівського технологічного інституту KTH.
Анна Герланд, старший автор дослідження, сказала, що дослідження продемонструвало перше використання мікрофлюїдики для перетворення iPSC на нейронні стовбурові клітини.
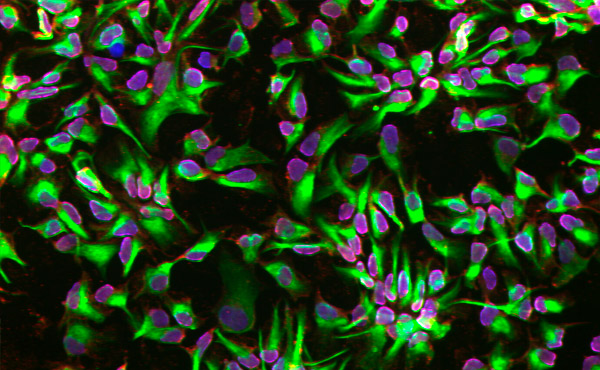
Нейронні стовбурові клітини диференціюються за допомогою мікрофлюїдної платформи. Фото: Королівський технологічний інститут KTH
Трансформація нормальних клітин у нейронні стовбурові клітини насправді є двоетапним процесом. Спочатку клітини піддаються впливу біохімічних сигналів, які спонукають їх стати плюрипотентними стовбуровими клітинами (iPSC), які можуть генерувати різні типи клітин.
Потім їх переносять у культуру, яка імітує сигнали та процеси розвитку, що беруть участь у формуванні нервової системи. Цей крок, який називається нейронною диференціацією, перенаправляє клітини у напрямку перетворення на нейронні стовбурові клітини.
Протягом останнього десятиліття лабораторне середовище для такого типу роботи поступово перейшло від традиційних планшетів до мікрофлюїдних пристроїв. Герланд каже, що нова платформа являє собою вдосконалення в мікрофлюїдіці для обох етапів: генерації iPSC та диференціації нейронних стовбурових клітин.
Використовуючи клітини з біопсій шкіри людини, дослідники виявили, що мікрофлюїдна платформа прискорила закріплення клітин за нейронною системою на більш ранній стадії порівняно з тими, що диференціювалися у звичайних пластинах.
«Ми задокументували, що обмежене середовище мікрофлюїдної платформи посилює прагнення до створення нейронних стовбурових клітин», — каже Герланд.
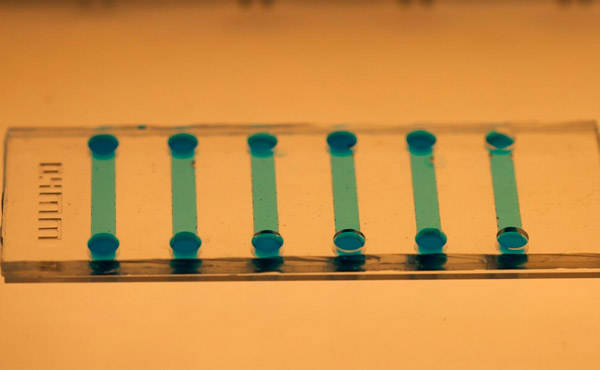
Крупний план мікрофлюїдного чіпа, що використовується для індукції стовбурових клітин. Фото: Королівський технологічний інститут KTH
Джайн каже, що мікрофлюїдний чіп легко виготовити з використанням полідиметилсилоксану (PDMS), а його мікроскопічний розмір дозволяє значно заощадити на реагентах та клітинному матеріалі.
Він додає, що платформу можна легко модифікувати для забезпечення диференціації в інші типи клітин. Її можна автоматизувати, забезпечуючи замкну систему, яка гарантує узгодженість та надійність у виробництві високооднорідних клітинних популяцій.
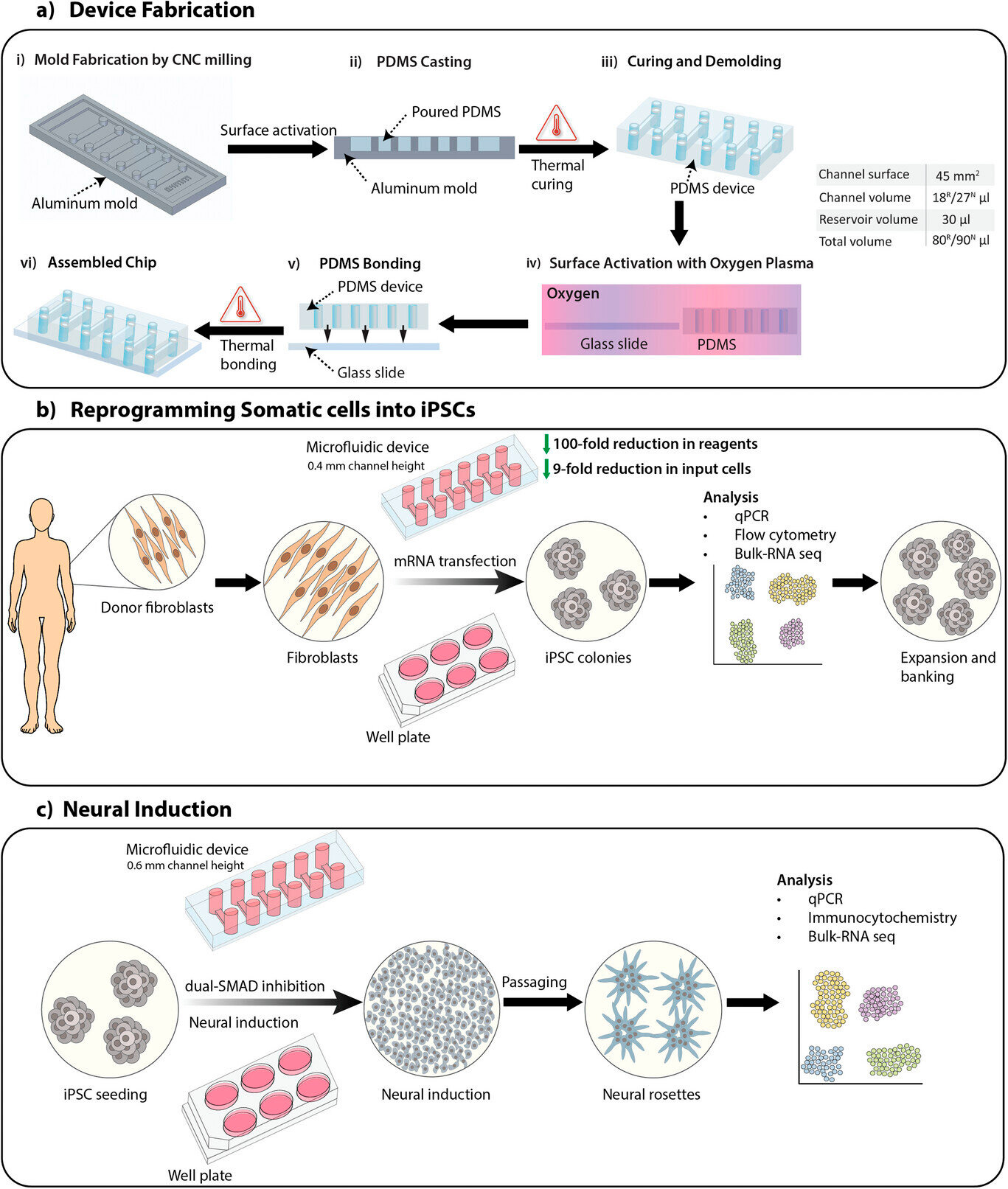
Огляд дослідження, включаючи виготовлення пристрою, перепрограмування соматичних клітин в індуковані плюрипотентні стовбурові клітини (iPSC) та нейронну індукцію iPSC з використанням протоколу подвійного інгібування SMAD для створення нейронних стовбурових клітин.
A) Процес виготовлення мікрофлюїдного пристрою з каналами висотою 0,4 мм та 0,6 мм для перепрограмування соматичних клітин (R) та нейронної індукції (N) відповідно. Об'єми каналів та загальний об'єм наведено в таблиці.
B) Огляд процесу перепрограмування соматичних клітин в iPSC на мікрофлюїдних пристроях та планшетах з використанням трансфекції мРНК.
C) Огляд процесу нейронної індукції iPSC у нейронні стовбурові клітини на мікрофлюїдних пристроях та планшетах з використанням протоколу подвійного інгібування SMAD.
Джерело: Advanced Science (2024). DOI: 10.1002/advs.202401859
«Це крок до того, щоб зробити персоналізовану клітинну терапію хвороб Альцгеймера та Паркінсона доступною», – додає Джайн.
У дослідженні також брали участь вчені з Каролінського інституту та Лундського університету, які співпрацювали в консорціумі IndiCell.
