Медичний експерт статті
Нові публікації
Артеріовенозна мальформація
Останній перегляд: 04.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
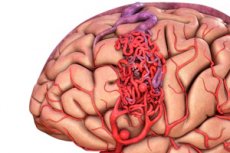
Артеріовенозна мальформація – це вроджений дефект розвитку кровоносних судин, який характеризується наявністю аномальної мережі артеріовенозних анастомозів. Найчастіше артеріовенозні мальформації розташовані в задній черепній ямці та мають досить типову структуру – одну або дві справжні артерії, клубок артеріовенозних мальформацій та одну дренуючу вену.
 [ 1 ]
[ 1 ]
Причини артеріовенозної мальформації
Причини, що можуть лежати в основі розвитку артеріовенозної мальформації (АВМ), до кінця не зрозумілі, але вважається, що вони можуть бути пов'язані з генетичними та екологічними факторами. Ось деякі з можливих причин, які можуть бути пов'язані з розвитком АВМ:
- Генетичні фактори: Дослідження показали, що деякі пацієнти з артеріовенозними мальформаціями (АВМ) мають сімейний анамнез цього захворювання. Генетичні мутації можуть відігравати певну роль у формуванні судинної аномалії.
- Вроджені вади: Вроджені судинні аномалії можуть розвиватися під час ембріонального розвитку. Вони можуть бути пов'язані з помилками у розвитку судинних тканин мозку.
- Фактори навколишнього середовища: Деякі дослідження показали зв'язок між артеріовенозними мальформаціями (АВМ) та певними факторами навколишнього середовища, такими як радіація або токсичний вплив під час вагітності. Однак ці зв'язки не завжди підтверджені та не пояснюють усі випадки АВМ.
- Регіональні фактори: У деяких випадках артеріовенозні мальформації (АВМ) можуть бути пов'язані з певними географічними районами або етнічними групами, але ці зв'язки потребують подальшого вивчення.
Окрім цих факторів, які можуть впливати на розвиток артеріовенозної мальформації (АВМ), важливо зазначити, що це вроджене захворювання, яке зазвичай виявляється при народженні або в ранньому дитинстві, хоча симптоми можуть з'явитися пізніше. Для точного розуміння причин та механізмів розвитку АВМ необхідні подальші дослідження.
Патогенез
Найбільш небезпечним є розрив стінок мальформації, який супроводжується спонтанним внутрішньочерепним крововиливом. Це відбувається через те, що в судинах мальформації циркулює змішана кров під тиском, близьким до артеріального. І природно, високий тиск призводить до розтягування дегенеративно змінених судин, збільшення їх об'єму та витончення стінки. Зрештою, розрив відбувається в найтоншому місці. За статистичними даними, це трапляється у 42-60% пацієнтів з артеріовенозною мальформацією (АВМ). Смертність при першому розриві АВМ досягає 12-15%. В решті кровотеча може повторюватися, без будь-якої періодичності. Ми спостерігали пацієнта, у якого протягом 8 років було одинадцять спонтанних внутрішньочерепних крововиливів. Такий відносно «доброякісний» перебіг розриву АВМ порівняно з розривом артеріальних аневризм пояснюється особливостями гемодинамічних порушень, що виникають після розриву. Відомо, що розрив артеріальної аневризми найчастіше призводить до субарахноїдального крововиливу (САК) та розвитку ангіоспазму, який у перші хвилини носить захисний характер, допомагаючи швидко зупинити кровотечу, але згодом становить велику небезпеку для життя пацієнта.
Саме ангіоспазм, що призводить до ішемії головного мозку та набряку, визначає тяжкість стану пацієнта та прогноз. Натомість, ангіоспазм приносних артерій артеріовенозної мальформації (АВМ), навпаки, покращує кровопостачання мозку завдяки зменшенню артеріовенозного скиду. При розриві АВМ частіше утворюються внутрішньомозкові та субдуральні гематоми. Прорив крові в субарахноїдальні цистерни є вторинним. Кровотеча з розірваної стінки АВМ зупиняється швидше, оскільки тиск крові в ній нижчий, ніж в основних артеріях, і стінка більш схильна до стиснення кров’ю, що вилилася. Природно, це не завжди закінчується добре для пацієнта. Найбільш небезпечні розриви АВМ відбуваються поблизу шлуночків мозку, у підкіркових гангліях та у стовбурі мозку. Ангіоспазм приносних артерій у цій ситуації допомагає зупинити кровотечу.
Визначальним фактором у патогенезі розриву артеріовенозної мальформації (АВМ) є об'єм крові, що вилилася, та локалізація гематоми. Півкульні внутрішньомозкові гематоми, навіть об'ємом до 60 см3 , протікають відносно сприятливо. Вони можуть спричиняти тяжкі вогнищеві неврологічні розлади, але рідко призводять до тяжких життєво важливих порушень. Розрив гематоми в шлуночки мозку значно погіршує прогноз. З одного боку, кров, подразнюючи епендиму шлуночків, збільшує продукцію спинномозкової рідини, з іншого боку, вражаючи дно шлуночка, призводить до тяжких порушень функцій життєво важливих центрів, розташованих у гіпоталамусі. Поширення крові по всій шлуночковій системі призводить до тампонади останніх, що саме по собі несумісне з життям.
Кров, що проникла в субарахноїдальні цистерни, також порушує циркуляцію спинномозкової рідини, ускладнюючи її надходження до закупорених кров’ю грануляцій пахіону. В результаті сповільнюється резорбція спинномозкової рідини та може розвинутися гостра лікворна гіпертензія, а потім внутрішня та зовнішня гідроцефалія. Внаслідок розпаду формених елементів крові, що вилилася, утворюється велика кількість токсичних речовин, більшість з яких мають вазоактивну дію. З одного боку, це призводить до вазоконстрикції дрібних піальних артерій, а з іншого – підвищує проникність капілярів. Продукти розпаду крові також впливають на нервові клітини, змінюючи їхні біохімічні процеси та порушуючи проникність клітинних мембран. Перш за все, змінюється функція калій-натрієвого насоса і калій починає виходити з клітини, а на його місце поспішає катіон натрію, який у чотири рази гідрофільніший за калій.
Це призводить спочатку до внутрішньоклітинного набряку в області навколо крововиливу, а потім до набряку клітин. Гіпоксія також сприяє розвитку набряку, який неминуче приєднується через здавлення судин мозку гематомою та підвищення тиску спинномозкової рідини, про що вже було сказано. Порушення функції діенцефальних відділів мозку та, перш за все, регуляції водно-електролітного балансу призводить до затримки рідини в організмі, втрати калію, що також посилює набрякову реакцію мозку. Патогенез розриву АВМ не обмежується лише церебральними порушеннями. Не менш небезпечними є позамозкові ускладнення. Перш за все, це цереброкардіальний синдром, який на електрокардіограмі може симулювати гостру коронарну недостатність.
Досить швидко у пацієнтів з внутрішньомозковими крововиливами розвивається пневмонія та дихальна недостатність. Причому бактеріальна флора відіграє вторинну роль. Первинний ефект – центральний вплив на легені, що полягає в поширеному бронхоспазмі, підвищеному виробленні мокротиння та слизу, ішемії легеневої паренхіми внаслідок поширеного спазму дрібних легеневих артерій, що швидко призводить до дистрофічних розладів, десквамації альвеолярного епітелію та зниження газообмінної функції легень.
Якщо це супроводжується пригніченням кашльового рефлексу, бульбарним типом дихальної недостатності, то виникає серйозна загроза життю пацієнта. У більшості випадків гнійний трахіобронхіт, що виник, погано піддається антибактеріальній терапії та посилює дихальну недостатність, що одразу впливає на наростання гіпоксії мозку. Таким чином, порушення зовнішнього дихання, навіть за умови відносної компенсації мозкових розладів, може призвести до летального результату. Нерідко хворі після коми приходять до тями, але потім помирають від наростаючої дихальної недостатності та гіпоксичного набряку мозку.
Дистрофічні зміни швидко розвиваються не лише в легенях, а й у печінці, шлунково-кишковому тракті, надниркових залозах та нирках. Інфекція сечовивідних шляхів та пролежні, які швидко розвиваються за відсутності належного догляду за пацієнтом, становлять загрозу для життя пацієнта. Але цих ускладнень можна уникнути, якщо лікарі пам’ятатимуть про них та знатимуть, як з ними боротися.
Підсумовуючи розгляд патогенезу розриву артеріовенозних мальформацій (АВМ), слід наголосити, що летальність при таких внутрішньочерепних крововиливах нижча, ніж при розриві артеріальних аневризм та гіпертонічних геморагічних інсультах, хоча й сягає 12-15%. АВМ характеризуються повторними, іноді множинними крововиливами з різною періодичністю, яку неможливо передбачити. У разі несприятливого перебігу постгеморагічного періоду перелічені патогенетичні механізми можуть призвести до летального результату.
Симптоми артеріовенозної мальформації
Геморагічний тип захворювання (50-70% випадків). Цей тип характеризується наявністю у пацієнта артеріальної гіпертензії, невеликим розміром вузла мальформації, його дренажем у глибокі вени, артеріовенозна мальформація задньої черепної ямки є досить поширеним явищем.
Геморагічний тип у 50% випадків є першим симптомом прояву артеріовенозної мальформації, спричиняє детальний результат та 10-15% інвалідність та 20-30% пацієнтів (Н. Мартін та ін.). Річний ризик крововиливу у пацієнтів з артеріовенозною мальформацією становить 1,5-3%. Ризик повторного крововиливу протягом першого року досягає 8% і зростає з віком. Кровотеча з артеріовенозної мальформації є причиною 5-12% всієї материнської смертності та 23% усіх внутрішньочерепних крововиливів у вагітних жінок. Картина субарахноїдального крововиливу спостерігається у 52% пацієнток. У 17% пацієнток виникають ускладнені форми крововиливу: формування внутрішньомозкових (38%), субдуральних (2%) та змішаних (13%) гематом, гемотампонада шлуночків розвивається у 47%.
Торпідний тип перебігу типовий для пацієнтів з великими артеріовенозними мальформаціями, локалізованими в кірковій речовині. Кровопостачання артеріовенозної мальформації забезпечується гілками середньої мозкової артерії.
Найбільш характерними симптомами торпідного типу перебігу є судомний синдром (у 26-27% пацієнтів з артеріовенозною мальформацією), кластерні головні болі та прогресуючий неврологічний дефіцит, як при пухлинах головного мозку.
Варіанти клінічних проявів артеріовенозних мальформацій
Як уже зазначалося, найпоширенішим першим клінічним проявом артеріовенозної мальформації (АВМ) є спонтанний внутрішньочерепний крововилив (у 40-60% пацієнтів). Він часто виникає без будь-яких провісників, на тлі повного здоров'я. Провокуючими моментами можуть бути фізичне навантаження, стресова ситуація, нервово-психічне напруження, прийом великих доз алкоголю тощо. У момент розриву АВМ пацієнти відчувають раптовий різкий головний біль, подібний до удару або розриву. Біль швидко посилюється, викликаючи запаморочення, нудоту та блювоту.

Втрата свідомості може статися протягом кількох хвилин. У рідкісних випадках головний біль може бути незначним, пацієнти не втрачають свідомість, але відчувають ослаблення та оніміння кінцівок (зазвичай контралатерально до місця крововиливу), а також порушення мови. У 15% випадків крововилив проявляється як повноцінний епілептичний напад, після якого пацієнти можуть залишатися в коматозному стані.
Для визначення тяжкості крововиливу з артеріовенозної мальформації (АВМ) за основу можна використовувати наведену вище шкалу Ханта-Гесса з деякими коригуваннями. З огляду на те, що крововиливи з АВМ можуть мати дуже різні симптоми, вогнищеві неврологічні симптоми можуть переважати над загальномозковими. Тому у пацієнтів з рівнем свідомості на I або II рівнях шкали можуть бути тяжкі вогнищеві неврологічні розлади (геміпарез, гемігіпестезія, афазія, геміанопсія). На відміну від аневризматичних крововиливів, розрив АВМ визначається не тяжкістю та поширеністю ангіоспазму, а об'ємом та локалізацією внутрішньомозкової гематоми.
Менінгеальний синдром розвивається через кілька годин, і його тяжкість може варіюватися. Артеріальний тиск зазвичай підвищується, але не так різко і не так довго, як при розривах артеріальних аневризм. Зазвичай це підвищення не перевищує 30-40 мм рт. ст. На другий-третій день з'являється гіпертермія центрального генезу. Стан пацієнтів закономірно погіршується, оскільки наростає набряк мозку та посилюється розпад вилитої крові. Це триває до 4-5 днів. При сприятливому перебігу, після стабілізації на 6-8-й день, стан пацієнтів починає покращуватися. Динаміка вогнищевих симптомів залежить від локалізації та розміру гематоми.
У разі крововиливу у функціонально важливі ділянки мозку або руйнування рухових провідників симптоми випадіння виникають негайно та зберігаються тривалий час без будь-якої динаміки. Якщо симптоми випадіння з'являються не одразу, а наростають паралельно з набряком мозку, можна очікувати відновлення дефіциту через 2-3 тижні, коли набряк повністю регресує.
Клінічна картина розриву артеріовенозної мальформації (АВМ) досить різноманітна та залежить від багатьох факторів, основними з яких є: обсяг та локалізація крововиливу, тяжкість реакції набряку мозку та ступінь залучення до процесу структур стовбура мозку.
Артеріовенозні мальформації можуть проявлятися епілептиформними судомами (30-40%). Причиною їх розвитку можуть бути гемоциркуляторні порушення в сусідніх ділянках мозку через феномен обкрадання. Крім того, сама мальформація може подразнювати кору головного мозку, генеруючи епілептичні розряди. І ми вже говорили про певні типи АВМ, навколо яких розвивається гліоз тканини мозку, що також часто проявляється епілептичними судомами.
Епілептичний синдром, спричинений наявністю артеріовенозної мальформації (АВМ), характеризується безпричинним виникненням у дорослому віці, часто за повної відсутності провокуючого фактора. Напади можуть бути генералізованими або вогнищевими. Наявність чіткого вогнищевого компонента при епілептичному нападі за відсутності загальномозкових симптомів повинна навести на думку про можливу АВМ. Навіть генералізовані напади, якщо вони починаються з судом переважно в тих самих кінцівках з вимушеним поворотом голови та очей в один чи інший бік, часто є проявом АВМ. Рідше у пацієнтів спостерігаються незначні напади, такі як абсанси або сутінкова свідомість. Частота та періодичність епілептичних нападів можуть варіюватися: від ізольованих до рецидивуючих.
Форми
В. В. Лебедєв та співавтори на основі даних ЕКГ визначили три варіанти цереброкардіального синдрому:
- I тип – порушення функцій автоматизму та збудливості (синусова тахікардія або брадикардія, аритмія, фібриляція передсердь);
- II тип – зміни процесів реполяризації, транзиторні зміни кінцевої фази шлуночкового комплексу за типом ішемії, ураження міокарда зі змінами зубця Т та положення сегмента ST;
- III тип – порушення провідної функції (блокада, ознаки підвищеного навантаження на праві відділи серця). Ці зміни ЕКГ можуть поєднуватися, а їхня тяжкість корелює з тяжкістю загального стану пацієнтів.
Ускладнення і наслідки
Артеріовенозна мальформація (АВМ) – це вроджена судинна аномалія, при якій артерії та вени з’єднані без проміжного капілярного шару. Ускладнення та наслідки АВМ можуть бути серйозними та залежать від розміру, розташування та характеристик конкретної мальформації. Деякі з них включають:
- Інсульт: Одним із найсерйозніших ускладнень артеріовенозних мальформацій (АВМ) є ризик інсульту. Вади розвитку можуть створювати аномальні шляхи кровотоку, що може призвести до кровотечі в мозку та спричинити інсульт. Інсульт може мати різний ступінь тяжкості та залишати залишкові неврологічні дефіцити.
- Епілепсія: АВМ можуть спричиняти епілептичні напади у деяких пацієнтів, особливо якщо мальформація розташована в певних ділянках мозку.
- Кровотеча: Вади розвитку можуть бути непередбачуваними та спричиняти кровотечу в мозку. Це може бути небезпечним для життя ускладненням і призвести до серйозних наслідків.
- Гідроцефалія: Якщо артеріовенозна мальформація розташована поблизу шлуночків мозку, це може спричинити гідроцефалію, яка може призвести до накопичення зайвої рідини в мозку та підвищення внутрішньочерепного тиску.
- Неврологічний дефіцит: АВМ може пошкодити навколишні тканини мозку та спричинити різноманітні неврологічні порушення, включаючи параліч, сенсорні порушення та порушення мовлення та моторної координації.
- Біль та головний біль: пацієнти з артеріовенозною мальформацією (АВМ) можуть відчувати хронічний біль та головний біль, пов’язані з мальформацією.
- Психологічні наслідки: Ускладнення від артеріовенозних мальформацій (АВМ) можуть суттєво впливати на психологічне благополуччя пацієнтів, включаючи тривогу, депресію та стрес.
- Обмеження способу життя: Після виявлення артеріовенозної мальформації пацієнтам можуть знадобитися зміни способу життя та рекомендації щодо управління ризиками, включаючи обмеження фізичної активності та певних видів діяльності.
Діагностика артеріовенозної мальформації
Діагностика артеріовенозної мальформації (АВМ) зазвичай включає різноманітні візуалізаційні тести для підтвердження наявності та оцінки характеристик мальформації. Основні методи, що використовуються для діагностики АВМ:
- Магнітно-резонансна ангіографія (МРА): МРА є одним з основних методів діагностики артеріовенозних мальформацій (АВМ). Це неінвазивний тест, який візуалізує структуру кровоносних судин та кровотік у мозку за допомогою магнітних полів та радіохвиль. МРА може визначити розташування, розмір та форму АВМ.
- Цифрова субтракційна ангіографія (ЦСА): це більш інвазивна процедура, яка передбачає введення контрастної речовини безпосередньо в судини через катетер та використання рентгенівських променів для отримання високоякісних зображень судин мозку. ЦСА дозволяє детальніше дослідити структуру артеріовенозних вен та картини кровотоку.
- Комп'ютерна томографія (КТ): КТ може бути використана для виявлення артеріовенозних мальформацій (АВМ) та оцінки можливих ускладнень, таких як кровотеча. За потреби для покращення візуалізації може бути використана контрастна речовина.
- Судинне дуплексне сканування (дуплексне ультразвукове дослідження): цей метод може бути корисним для дослідження судин шиї та голови та виявлення порушень кровотоку, пов'язаних з артеріовенозними мальформаціями (АВМ).
- Магнітно-резонансна спектроскопія (МРС): МРС може надати інформацію про хімічний склад тканин в області артеріовенозної мальформації та виявити ознаки метаболічних змін.
- Ехоенцефалографія: це ультразвукове дослідження, яке можна використовувати для оцінки кровотоку та структури мозку.
- Комп'ютерна томографія та ангіографія (КТА): КТА поєднує КТ та ангіографію для отримання тривимірних зображень кровоносних судин головного мозку.
Після встановлення діагнозу артеріовенозної мальформації (АВМ) важливо провести детальну оцінку характеристик мальформації, таких як її розмір, форма та тяжкість. Це допоможе визначити, чи потрібне лікування, та який варіант лікування найкращий, включаючи хірургічне видалення, емболізацію, променеву терапію або спостереження. Рішення про лікування АВМ має прийматися спільно між пацієнтом та медичною командою, враховуючи індивідуальні обставини кожного випадку.
Диференціальна діагностика
Диференціальна діагностика артеріовенозних мальформацій (АВМ) може бути важливим кроком в обстеженні пацієнта із судинними змінами в головному мозку. АВМ – це судинні аномалії, при яких артерії та вени з’єднані без проміжного капілярного шару. Вони можуть спричиняти різноманітні симптоми та стани, і їх диференціація від інших судинних захворювань важлива для правильного лікування. Деякі стани, які можуть вимагати диференціальної діагностики з АВМ, включають:
- Інсульт: Інсульти можуть імітувати симптоми артеріовенозної мальформації (АВМ), особливо якщо інсульт спричинений судинними змінами. Для візуалізації судинних змін може знадобитися комп’ютерна томографія (КТ) або магнітно-резонансна томографія (МРТ) головного мозку.
- Гематома: Гематоми, такі як субдуральна або епідуральна гематома, можуть імітувати симптоми артеріовенозної мальформації (АВМ), особливо якщо вони супроводжуються головним болем та неврологічними симптомами. КТ або МРТ можуть допомогти визначити причину симптомів.
- Пухлини головного мозку: Пухлини головного мозку можуть викликати різноманітні симптоми, подібні до симптомів артеріовенозної мальформації (АВМ). Діагностика може включати МРТ з контрастом та інші дослідження візуалізації.
- Мігрень: Мігрень з аурою може імітувати симптоми артеріовенозної мальформації (АВМ), такі як порушення зору та запаморочення. Анамнез та додаткові обстеження можуть допомогти розрізнити ці два стани.
- Церебральний васкуліт: Васкуліт може спричинити запалення кровоносних судин та судинні порушення, які можуть імітувати симптоми артеріовенозної мальформації (АВМ). Для діагностики васкуліту може бути використана біопсія або ангіографія.
- Венозний тромбоз: Венозні тромбози можуть імітувати симптоми артеріовенозної мальформації (АВМ), особливо якщо є порушення венозного відтоку від мозку. Додаткові дослідження можуть допомогти у виявленні тромбозу.
Для точної диференціальної діагностики артеріовенозних мальформацій (АВМ) обстеження включає ретельне клінічне обстеження, нейроосвітні методи (КТ, МРТ, ангіографію), іноді біопсію та інші спеціалізовані процедури залежно від конкретних симптомів та обставин.
До кого звернутись?
Лікування артеріовенозної мальформації
Лікування артеріовенозної мальформації (АВМ) залежить від її розміру, розташування, симптомів та потенційних ускладнень. У деяких випадках АВМ може бути невеликою та безсимптомною, і може не потребувати активного лікування. Однак, якщо є симптоми або ризик кровотечі, лікування може бути необхідним. Деякі методи лікування АВМ включають:
- Хірургічне втручання: Хірургічне видалення артеріовенозної мальформації може розглядатися у випадках, коли мальформація знаходиться в доступному місці та не має складності. Хірургічне видалення може допомогти запобігти ризику кровотечі та зменшити симптоми. Це складна процедура, яка може нести такі ризики, як пошкодження навколишніх тканин і нервів.
Відкриті (транскраніальні) втручання:
- I стадія – коагуляція аферентних волокон;
- II стадія – виділення ядра артеріовенозної мальформації;
- III стадія - лігування та коагуляція еферентної протоки та видалення артеріовенозної мальформації,
Ендоваскулярні втручання:
- стаціонарна балонна оклюзія живлячих артерій - емболізація всередині потоку (неконтрольована);
- поєднання тимчасової або постійної балонної оклюзії з емболізацією потоком;
- суперселективна емболізація.
Артеріовенозну мальформацію також лікують за допомогою радіохірургії (гамма-ніж, кібер-ніж, Лінак тощо).
- Емболізація: Емболізація – це процедура, під час якої медичні матеріали або клей вводяться в кровоносні судини для блокування кровотоку до артеріовенозної мальформації (АВМ). Емболізацію можна використовувати як підготовчий крок перед операцією або як самостійний метод лікування. Вона може допомогти зменшити кровотечу та розмір АВМ.
- Променева терапія: Променева терапія може використовуватися для лікування артеріовенозних мальформацій (АВМ), особливо у випадках, коли інші методи лікування можуть бути занадто ризикованими. Променева терапія спрямована на зменшення кровотечі з АВМ і може вимагати кількох сеансів.
- Ліки: У деяких випадках ліки можуть використовуватися для зменшення таких симптомів, як біль або спазми. Ліки також можуть використовуватися для контролю артеріального тиску, щоб зменшити ризик кровотечі.
- Спостереження та лікування симптомів: У деяких ситуаціях, особливо якщо АВМ невелика та не викликає симптомів, може бути прийнято рішення просто спостерігати за станом та лікувати симптоми за потреби.
Лікування артеріовенозних мальформацій (АВМ) має бути індивідуалізованим для кожного пацієнта, а рішення щодо вибору методу залежить від конкретних обставин. Важливо обговорити всі варіанти лікування з медичним працівником та провести ретельне обстеження пацієнта, щоб визначити найкращий план лікування. Результати лікування можуть бути успішними, і пацієнти можуть досягти покращення або повного одужання, але кожен випадок унікальний.
Прогноз
Прогноз артеріовенозної мальформації (АВМ) залежить від кількох факторів, включаючи її розмір, розташування, симптоми, вік пацієнта та успішність лікування. Важливо пам’ятати, що АВМ – це захворювання, яке може проявлятися по-різному у різних пацієнтів, і прогноз може відрізнятися від людини до людини. Ось деякі загальні аспекти прогнозу АВМ:
- Ризик кровотечі: Основним ризиком артеріовенозної мальформації (АВМ) є ризик кровотечі (крововиливу) в мозок. Невеликі АВМ з низьким ризиком кровотечі можуть мати хороший прогноз і не спричиняти серйозних проблем. Однак великі та середні АВМ можуть становити значний ризик.
- Симптоми: Симптоми, пов'язані з артеріовенозною мальформацією (АВМ), такі як головний біль, судоми, параліч або сенсорні порушення, можуть впливати на прогноз. У деяких випадках успішне лікування може покращити або усунути симптоми.
- Розмір і розташування: артеріовенозні мальформації (АВМ), розташовані в більш небезпечних місцях, таких як глибоко в мозку або поблизу критичних структур, можуть мати гірший прогноз. Однак навіть багато великих АВМ можна успішно лікувати.
- Лікування: Лікування артеріовенозних мальформацій може включати хірургічне видалення, емболізацію, променеву терапію або медикаментозне лікування. Успішне лікування може зменшити ризик кровотечі та покращити прогноз.
- Вік: Вік пацієнта також може впливати на прогноз. Діти та молоді люди часто мають кращий прогноз, ніж пацієнти старшого віку.
- Супутні захворювання: Наявність інших захворювань або факторів ризику, таких як високий кров'яний тиск або порушення згортання крові, може впливати на прогноз та лікування артеріовенозної мальформації (АВМ).
Важливо зазначити, що артеріовенозно-весняна мальформація (АВМ) потребує ретельного медичного спостереження та лікування. Рішення щодо методу лікування та прогнозу повинні приймати кваліфіковані нейрохірурги та нейрорадіологи на основі ретельної оцінки кожного окремого випадку.

