Медичний експерт статті
Нові публікації
Діагностика остеоартрозу: магнітно-резонансна томографія
Останній перегляд: 04.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
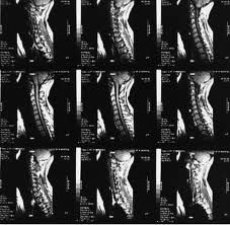
Магнітно-резонансна томографія (МРТ) стала одним з провідних методів неінвазивної діагностики остеоартриту в останні роки. З 1970-х років, коли принципи магнітного резонансу (МРТ) були вперше використані для дослідження людського організму, цей метод медичної візуалізації кардинально змінився та продовжує швидко розвиватися.
Удосконалюється технічне обладнання та програмне забезпечення, розробляються методи отримання зображень, розробляються контрастні речовини для МРТ. Це дозволяє постійно знаходити нові сфери застосування МРТ. Якщо спочатку її застосування обмежувалося дослідженнями центральної нервової системи, то зараз МРТ успішно використовується майже у всіх галузях медицини.
У 1946 році групи дослідників зі Стенфордського та Гарвардського університетів незалежно одна від одної відкрили явище, яке називається ядерним магнітним резонансом (ЯМР). Його суть полягала в тому, що ядра деяких атомів, перебуваючи в магнітному полі, під впливом зовнішнього електромагнітного поля здатні поглинати енергію, а потім випромінювати її у вигляді радіосигналу. За це відкриття Ф. Блох та Е. Пармель були удостоєні Нобелівської премії в 1952 році. Нове явище незабаром було використано для спектрального аналізу біологічних структур (ЯМР-спектроскопія). У 1973 році Пауль Раутенбург вперше продемонстрував можливість отримання зображення за допомогою ЯМР-сигналів. Так з'явилася ЯМР-томографія. Перші ЯМР-томограми внутрішніх органів живої людини були продемонстровані в 1982 році на Міжнародному конгресі радіологів у Парижі.
Слід дати два уточнення. Незважаючи на те, що метод базується на явищі ЯМР, його називають магнітним резонансом (МР), опускаючи слово «ядерний». Це зроблено для того, щоб у пацієнтів не виникало думок про радіоактивність, пов’язану з розпадом атомних ядер. І друга обставина: МР-томографи випадково не «налаштовані» на протони, тобто ядра водню. Цього елемента в тканинах багато, а його ядра мають найбільший магнітний момент серед усіх атомних ядер, що визначає досить високий рівень МР-сигналу.
Якщо в 1983 році у світі було лише кілька приладів, придатних для клінічних досліджень, то до початку 1996 року у світі експлуатувалося близько 10 000 томографів. Щороку в практику впроваджується 1000 нових приладів. Понад 90% парку МР-томографів – це моделі з надпровідними магнітами (0,5-1,5 Тл). Цікаво відзначити, що якщо в середині 80-х років компанії – виробники МР-томографів керувалися принципом «чим вище поле, тим краще», зосереджуючись на моделях з полем 1,5 Тл і вище, то до кінця 80-х років стало зрозуміло, що в більшості областей застосування вони не мають суттєвих переваг перед моделями із середньою напруженістю поля. Тому основні виробники МР-томографів (General Electric, Siemens, Philips, Toshiba, Picker, Bruker та ін.) наразі приділяють значну увагу виробництву моделей із середніми та навіть низькими полями, які відрізняються від високопольових систем своєю компактністю та економічністю при задовільній якості зображення та значно нижчій вартості. Високопольові системи використовуються переважно в дослідницьких центрах для МР-спектроскопії.
Принцип методу МРТ
Основними компонентами МРТ-сканера є: надсильний магніт, радіопередавач, приймальна радіочастотна котушка, комп'ютер і панель керування. Більшість пристроїв мають магнітне поле з магнітним моментом, паралельним поздовжній осі людського тіла. Напруженість магнітного поля вимірюється в теслах (Тл). Для клінічної МРТ використовуються поля напруженістю 0,2-1,5 Тл.
Коли пацієнта поміщають у сильне магнітне поле, всі протони, які є магнітними диполями, повертаються в напрямку зовнішнього поля (як стрілка компаса, орієнтована до магнітного поля Землі). Крім того, магнітні осі кожного протона починають обертатися навколо напрямку зовнішнього магнітного поля. Цей специфічний обертальний рух називається процесією, а його частота - резонансною частотою. Коли через тіло пацієнта проходять короткі електромагнітні радіочастотні імпульси, магнітне поле радіохвиль змушує магнітні моменти всіх протонів обертатися навколо магнітного моменту зовнішнього поля. Для цього частота радіохвиль повинна дорівнювати резонансній частоті протонів. Це явище називається магнітним резонансом. Щоб змінити орієнтацію магнітних протонів, магнітні поля протонів і радіохвиль повинні резонувати, тобто мати однакову частоту.
У тканинах пацієнта створюється результуючий магнітний момент: тканини намагнічуються, а їхній магнетизм орієнтований строго паралельно зовнішньому магнітному полю. Магнетизм пропорційний кількості протонів на одиницю об'єму тканини. Величезна кількість протонів (ядер водню), що містяться в більшості тканин, означає, що результуючий магнітний момент достатньо великий, щоб індукувати електричний струм у приймальній котушці, розташованій поза пацієнтом. Ці індуковані МРТ-сигнали використовуються для реконструкції МРТ-зображення.
Процес переходу електронів ядра зі збудженого стану в рівноважний називається процесом спін-ґраткової релаксації або поздовжньої релаксації. Він характеризується T1 - часом спін-ґраткової релаксації - часом, необхідним для переведення 63% ядер у рівноважний стан після їх збудження імпульсом 90°. Також розрізняють T2 - час спін-спінової релаксації.
Існує кілька методів отримання МР-томограм. Вони відрізняються порядком та характером генерації радіочастотних імпульсів, а також методами аналізу МР-сигналу. Два найпоширеніші методи - це спін-ґратковий та спін-ехо. Спін-ґратковий метод в основному аналізує час релаксації T1. Різні тканини (сіра та біла речовина мозку, спинномозкова рідина, пухлинна тканина, хрящі, м'язи тощо) містять протони з різним часом релаксації T1. Інтенсивність МР-сигналу пов'язана з тривалістю T1: чим коротший T1, тим інтенсивніший МР-сигнал і тим яскравіше відображається дана область зображення на телевізійному моніторі. Жирова тканина на МР-томограмах має білий колір, за нею йдуть головний та спинний мозок, щільні внутрішні органи, судинні стінки та м'язи в порядку спадання інтенсивності МР-сигналу. Повітря, кістки та кальцифікати практично не створюють МР-сигнал і тому відображаються чорним кольором. Ці співвідношення часу релаксації T1 створюють передумови для візуалізації нормальних та змінених тканин на МРТ-сканах.
В іншому методі МРТ, який називається спін-ехо, на пацієнта спрямовується серія радіочастотних імпульсів, що обертають прецесуючи протони на 90°. Після припинення імпульсів реєструються сигнали МРТ-відповіді. Однак інтенсивність сигналу-відповіді по-різному пов'язана з тривалістю T2: чим коротший T2, тим слабший сигнал і, отже, тим нижча яскравість світіння на екрані телевізійного монітора. Таким чином, кінцева картина МРТ, отримана за допомогою методу T2, є протилежною до картини, отриманої за допомогою методу T1 (оскільки негатив є протилежністю позитивного).
МРТ-томограми краще відображають м’які тканини, ніж КТ: м’язи, жирові прошарки, хрящі та кровоносні судини. Деякі прилади можуть створювати зображення кровоносних судин без введення контрастної речовини (МРТ-ангіографія). Через низький вміст води в кістковій тканині остання не створює екрануючого ефекту, як при рентгенівській КТ, тобто не заважає зображенню, наприклад, спинного мозку, міжхребцевих дисків тощо. Звичайно, ядра водню містяться не тільки у воді, але й у кістковій тканині вони зафіксовані в дуже великих молекулах і щільних структурах і не заважають МРТ.
Переваги та недоліки МРТ
До основних переваг МРТ належать неінвазивність, нешкідливість (відсутність радіаційного навантаження), тривимірний характер отримання зображення, природний контраст від рухомої крові, відсутність артефактів від кісткової тканини, висока диференціація м'яких тканин, можливість виконання МП-спектроскопії для досліджень тканинного метаболізму in vivo. МРТ дозволяє отримувати зображення тонких шарів тіла людини в будь-якому перерізі - у фронтальній, сагітальній, аксіальній та косій площинах. Можлива реконструкція об'ємних зображень органів, синхронізація отримання томограм із зубцями електрокардіограми.
До основних недоліків зазвичай належать відносно тривалий час, необхідний для отримання зображень (зазвичай хвилини), що призводить до появи артефактів від дихальних рухів (це особливо знижує ефективність обстеження легень), аритмії (при кардіологічному обстеженні), неможливість достовірно виявляти камені, кальцифікати, деякі види кісткової патології, висока вартість обладнання та його експлуатації, особливі вимоги до приміщення, в якому розташовані прилади (екранування від перешкод), неможливість обстеження пацієнтів з клаустрофобією, штучні кардіостимулятори, великі металеві імплантати з немедичних металів.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Контрастні речовини для МРТ
На початку використання МРТ вважалося, що природний контраст між різними тканинами усуває потребу в контрастних речовинах. Невдовзі було виявлено, що різницю в сигналах між різними тканинами, тобто контрастність МРТ-зображення, можна значно покращити за допомогою контрастних речовин. Коли перший МРТ-контрастний агент (що містить парамагнітні іони гадолінію) став комерційно доступним, діагностична інформативність МРТ значно зросла. Суть використання МРТ-контрастних агентів полягає у зміні магнітних параметрів протонів тканин та органів, тобто у зміні часу релаксації (ЧР) протонів T1 та T2. Сьогодні існує кілька класифікацій МРТ-контрастних агентів (або точніше контрастних речовин - КАР).
За переважним впливом на час релаксації, MR-KA поділяється на:
- T1-CA, які скорочують T1 і тим самим збільшують інтенсивність сигналу тканинного MP. Їх також називають позитивними CA.
- Т2-КА, що скорочують Т2, зменшуючи інтенсивність МРТ-сигналу. Це негативні КА.
Залежно від магнітних властивостей, МР-КА поділяються на парамагнітні та суперпарамагнітні:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Парамагнітні контрастні речовини
Парамагнітними властивостями володіють атоми з одним або кількома неспареними електронами. Це магнітні іони гадолінію (Gd), хрому, нікелю, заліза та марганцю. Сполуки гадолінію отримали найширше клінічне застосування. Контрастний ефект гадолінію зумовлений скороченням часу релаксації T1 та T2. У низьких дозах переважає вплив на T1, що збільшує інтенсивність сигналу. У високих дозах переважає вплив на T2, що зменшує інтенсивність сигналу. Парамагнетики зараз найбільш широко використовуються в клінічній діагностичній практиці.
Суперпарамагнітні контрастні речовини
Домінуючим ефектом суперпарамагнітного оксиду заліза є скорочення Т2-релаксації. Зі збільшенням дози спостерігається зменшення інтенсивності сигналу. До цієї групи КА також можна віднести феромагнітні оксиди заліза, до яких належать феромагнітні оксиди заліза, структурно подібні до магнетитового фериту ( Fe2 + OFe23+ O3 ).
Наступна класифікація базується на фармакокінетиці КА (Сергеєв П.В. та ін., 1995):
- позаклітинний (тканинонеспецифічний);
- шлунково-кишковий тракт;
- органотропний (тканиноспецифічний);
- макромолекулярні, які використовуються для визначення судинного простору.
В Україні відомі чотири МР-КА, що являють собою позаклітинні водорозчинні парамагнітні КА, з яких широко використовуються гадодіамід та гадопентетова кислота. Решта груп КА (2-4) проходять клінічні випробування за кордоном.
Позаклітинний водорозчинний MR-CA
Міжнародна назва |
Хімічна формула |
Структура |
Гадопентетова кислота |
Гадолінію димеглумін діетилентріамін пентаацетат ((NMG)2Gd-DTPA) |
Лінійний, іонний |
Гадотерова кислота |
(NMG)Gd-DOTA |
Циклічні, іонні |
Гадодіамід |
Гадолінію діетилентріамінпентаацетат-біс-метиламід (Gd-DTPA-BMA) |
Лінійний, неіонний |
Гадотеридол |
Gd-HP-D03A |
Циклічні, неіонні |
Позаклітинні КА вводяться внутрішньовенно, 98% з них виводяться нирками, не проникають через гематоенцефалічний бар'єр, мають низьку токсичність та належать до групи парамагнітних речовин.
Протипоказання до МРТ
До абсолютних протипоказань належать стани, за яких обстеження становить загрозу для життя пацієнтів. Наприклад, наявність імплантів, що активуються електронно, магнітно або механічно – це, перш за все, штучні кардіостимулятори. Вплив радіочастотного випромінювання від МРТ-сканера може порушити функціонування кардіостимулятора, що працює в системі запиту, оскільки зміни магнітних полів можуть імітувати серцеву діяльність. Магнітне тяжіння також може призвести до зміщення кардіостимулятора в його гнізді та руху електродів. Крім того, магнітне поле створює перешкоди для роботи феромагнітних або електронних імплантів середнього вуха. Наявність штучних клапанів серця небезпечна та є абсолютним протипоказанням лише при обстеженні на МРТ-сканерах з високими полями, а також якщо клінічно підозрюється пошкодження клапана. До абсолютних протипоказань до обстеження також належить наявність невеликих металевих хірургічних імплантів (гемостатичних кліпс) у центральній нервовій системі, оскільки їх зміщення через магнітне тяжіння загрожує кровотечею. Їхня присутність в інших частинах тіла становить меншу загрозу, оскільки після лікування фіброз та інкапсуляція затискачів допомагають зберегти їх стабільність. Однак, окрім потенційної небезпеки, наявність металевих імплантатів з магнітними властивостями в будь-якому випадку спричиняє артефакти, що створюють труднощі в інтерпретації результатів дослідження.
Протипоказання до МРТ
Абсолютний: |
Родич: |
Кардіостимулятори |
Інші стимулятори (інсулінові помпи, нервові стимулятори) |
Феромагнітні або електронні імплантати середнього вуха |
Неферомагнітні імплантати внутрішнього вуха, протези серцевих клапанів (у високих полях, якщо підозрюється дисфункція) |
Гемостатичні кліпси судин головного мозку |
Гемостатичні кліпси в інших місцях, декомпенсована серцева недостатність, вагітність, клаустрофобія, потреба у фізіологічному моніторингу |
До відносних протипоказань, крім перелічених вище, належать декомпенсована серцева недостатність, необхідність фізіологічного моніторингу (штучна вентиляція легень, електричні інфузійні насоси). Клаустрофобія є перешкодою для дослідження в 1-4% випадків. Її можна подолати, з одного боку, використанням приладів з відкритими магнітами, з іншого - детальним поясненням приладу та ходу обстеження. Немає доказів шкідливого впливу МРТ на ембріон чи плід, але рекомендується уникати МРТ у першому триместрі вагітності. Застосування МРТ під час вагітності показано у випадках, коли інші неіонізуючі методи діагностичної візуалізації не дають задовільної інформації. МРТ-дослідження вимагає більшої участі пацієнта, ніж комп'ютерна томографія, оскільки рухи пацієнта під час обстеження значно більший вплив на якість зображень, тому обстеження пацієнтів з гострою патологією, порушенням свідомості, спастичними станами, деменцією, а також дітей часто буває утрудненим.

