Медичний експерт статті
Нові публікації
Голчаста електроміографія
Останній перегляд: 06.07.2025

Весь контент iLive перевіряється медичними експертами, щоб забезпечити максимально можливу точність і відповідність фактам.
У нас є строгі правила щодо вибору джерел інформації та ми посилаємося тільки на авторитетні сайти, академічні дослідницькі інститути і, по можливості, доведені медичні дослідження. Зверніть увагу, що цифри в дужках ([1], [2] і т. д.) є інтерактивними посиланнями на такі дослідження.
Якщо ви вважаєте, що який-небудь з наших матеріалів є неточним, застарілим або іншим чином сумнівним, виберіть його і натисніть Ctrl + Enter.
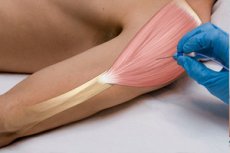
Голкова електроміографія включає такі основні методи:
- стандартна голкова ЕМГ;
- ЕМГ одного м'язового волокна;
- макроЕМГ;
- скануюча ЕМГ.
Стандартна голкова електроміографія
Голкова електроміографія – це інвазивний метод обстеження, що проводиться за допомогою концентричного голчастого електрода, що вводиться в м’яз. Голкова електроміографія дозволяє оцінити периферичний нейромоторний апарат: морфофункціональну організацію рухових одиниць скелетних м’язів, стан м’язових волокон (їх спонтанну активність), а за умови динамічного спостереження – оцінити ефективність лікування, динаміку патологічного процесу та прогноз захворювання.
Діагностичне значення
Стандартна голкова електроміографія займає центральне місце серед електрофізіологічних методів дослідження при різних нервово-м'язових захворюваннях і має вирішальне значення в диференціальній діагностиці нейрогенних та первинних м'язових захворювань.
Цей метод використовується для визначення ступеня денервації в м'язі, іннервованому ураженим нервом, ступеня його відновлення та ефективності реіннервації.
Голкова електроміографія знайшла своє застосування не лише в неврології, а й у ревматології, ендокринології, спортивній та професійній медицині, педіатрії, урології, гінекології, хірургії та нейрохірургії, офтальмології, стоматології та щелепно-лицевій хірургії, ортопедії та ряді інших медичних галузей.
Показання
Захворювання рухових нейронів спинного мозку ( БАС, спінальні аміотрофії, поліомієліт та постполіомієлітний синдром, сирингомієлія тощо), мієлопатії, радикулопатії, різні нейропатії (аксональні та демієлінізуючі), міопатії, запальні захворювання м'язів ( поліміозит та дерматоміозит ), центральні рухові розлади, розлади сфінктера та ряд інших ситуацій, коли необхідно об'єктивувати стан рухових функцій та системи контролю рухів, оцінити залученість у процес різних структур периферичного нейромоторного апарату.
 [ 6 ]
[ 6 ]
Підготовка
Пацієнту не потрібна жодна спеціальна підготовка до обстеження. Голкова електроміографія вимагає повного розслаблення м’язів, що досліджуються, тому її проводять у положенні пацієнта лежачи. Пацієнту піддають вплив м’язів, що досліджуються, укладають його на спину (або живіт) на зручну м’яку кушетку з регульованим підголівником, повідомляють про майбутнє обстеження та пояснюють, як слід напружувати, а потім розслабляти м’яз.
 [ 7 ]
[ 7 ]
Техніка голчастої електроміографії
Дослідження проводиться за допомогою концентричного голчастого електрода, що вводиться в рухову точку м'яза (допустимий радіус не більше 1 см для великих м'язів і 0,5 см для малих). Реєструються потенціали МО (ПМО). При виборі ПМО для аналізу необхідно дотримуватися певних правил їх відбору.
Багаторазові голчасті електроди попередньо стерилізують в автоклаві або іншими методами стерилізації. Одноразові стерильні голчасті електроди відкривають безпосередньо перед дослідженням м'язів.
Після введення електрода в повністю розслаблений м'яз і кожного його руху контролюється можлива поява спонтанної активності. PMU реєструється при мінімальному довільному напрузі м'язів, що дозволяє ідентифікувати окремі PMU. Вибираються 20 різних PMU, спостерігаючи певну послідовність руху електрода в м'язі.
При оцінці стану м'язів проводиться кількісний аналіз виявленої спонтанної активності, що особливо важливо при моніторингу стану пацієнта з плином часу, а також при визначенні ефективності терапії. Аналізуються параметри зареєстрованих потенціалів різних рухових одиниць.
Голкова електроміографія при синаптичних захворюваннях
При синаптичних захворюваннях голкову електроміографію вважають додатковим методом обстеження. При міастенії вона дозволяє оцінити ступінь «блокування» м’язових волокон у МУ, що визначається ступенем зменшення середньої тривалості МУ в досліджуваних м’язах. Однак головною метою голкової електроміографії при міастенії є виключення можливої супутньої патології (поліміозит, міопатія, ендокринні порушення, різні полінейропатії тощо). Голкову електроміографію у пацієнтів з міастенією також використовують для визначення ступеня реакції на введення антихолінестеразних препаратів, тобто для оцінки зміни параметрів МУ при введенні неостигміну метилсульфату (прозерину). Після введення препарату тривалість МУ в більшості випадків збільшується. Відсутність реакції може свідчити про так звану міастенічну міопатію.
Основні електроміографічні критерії синаптичних захворювань:
- скорочення середньої тривалості диференціального рівняння в часткових виробах;
- зменшення амплітуди окремих ПМУ (може бути відсутнім);
- помірна поліфазія ПДЕ (може бути відсутньою);
- відсутність спонтанної активності або наявність лише ізольованого ПФ.
При міастенії середня тривалість середньої тривалості середньої амплітуди сплесків заднього плану (МПВП) зазвичай незначно скорочена (на 10-35%). Більшість МПВП мають нормальну амплітуду, але в кожному м'язі реєструється кілька МПВП зниженої амплітуди та тривалості. Кількість поліфазних МПВП не перевищує 15-20%. Спонтанна активність відсутня. Якщо у пацієнта виявлено виражену ФП, слід розглянути поєднання міастенії з гіпотиреозом, поліміозитом або іншими захворюваннями.
Голкова електроміографія при первинних м'язових захворюваннях
Голкова електроміографія є основним електрофізіологічним методом діагностики первинних м'язових захворювань (різних міопатій). Через знижену здатність рухових одиниць розвивати достатню силу для підтримки навіть мінімальних зусиль, пацієнту з будь-якою первинною м'язовою патологією доводиться залучати велику кількість рухових одиниць. Це визначає особливість електроміографії у таких пацієнтів. При мінімальному довільному напрузі м'язів важко виділити окремі рухові одиниці; на екрані з'являється така безліч малих потенціалів, що їх ідентифікація стає неможливою. Це так звана міопатична картина електроміографії.
При запальних міопатіях (поліміозиті) відбувається процес реіннервації, що може спричинити підвищення параметрів MUAP.
Основні електроміографічні критерії первинних м'язових захворювань:
- скорочення середньої тривалості PDE більш ніж на 12%;
- зменшення амплітуди окремих ПМУ (середня амплітуда може бути як зниженою, так і нормальною, а іноді й підвищеною);
- поліфазія ПДЕ;
- виражена спонтанна активність м’язових волокон при запальній міопатії (поліміозиті) або ПМД (в інших випадках вона мінімальна або відсутня).
Зменшення середньої тривалості середньої тривалості MUAP є кардинальною ознакою будь-якого первинного м'язового захворювання. Причина цієї зміни полягає в тому, що при міопатіях м'язові волокна зазнають атрофії, деякі з них випадають зі складу MU через некроз, що призводить до зниження параметрів MUAP. Зменшення тривалості більшості MUAP виявляється майже у всіх м'язах пацієнтів з міопатіями, хоча воно більш виражене в клінічно найбільш уражених проксимальних м'язах.
Гістограма розподілу ПМУ за тривалістю зміщується в бік менших значень (стадія I або II). Винятком є ПМД: через різку поліфазію ПМУ, що іноді досягає 100%, середня тривалість може бути значно збільшена.
Електроміографія окремих м'язових волокон
Електроміографія окремих м'язових волокон дозволяє вивчати електричну активність окремих м'язових волокон, включаючи визначення їх щільності в м'язово-рухових одиницях та надійності нервово-м'язової передачі за допомогою методу тремтіння.
Для проведення дослідження потрібен спеціальний електрод з дуже малою поверхнею розряду діаметром 25 мкм, розташований на його бічній поверхні за 3 мм від кінця. Мала поверхня розряду дозволяє реєструвати потенціали одного м'язового волокна в зоні радіусом 300 мкм.
Дослідження щільності м'язових волокон
Визначення щільності м'язових волокон у МО базується на тому, що зона мікроелектрода для реєстрації активності окремого м'язового волокна суворо визначена. Мірою щільності м'язових волокон у МО є середня кількість потенціалів окремих м'язових волокон, зареєстрованих у зоні її реєстрації під час дослідження 20 різних МО в різних зонах м'яза. Зазвичай ця зона може містити лише одне (рідко два) м'язові волокна, що належать до однієї МО. Використовуючи спеціальний методичний прийом (тригерний пристрій), можна уникнути появи на екрані потенціалів окремих м'язових волокон, що належать до інших МО.
Середня щільність волокон вимірюється в умовних одиницях шляхом обчислення середньої кількості потенціалів окремих м'язових волокон, що належать до різних МО. У здорових людей це значення змінюється залежно від м'яза та віку від 1,2 до 1,8. Збільшення щільності м'язових волокон у МО відображає зміну структури МО в м'язі.
Дослідження феномену джиттера
Зазвичай завжди можливо розташувати електрод для реєстрації одного м'язового волокна в м'язі таким чином, щоб реєструвалися потенціали двох сусідніх м'язових волокон, що належать до однієї рухової одиниці. Якщо потенціал першого волокна активується пусковим пристроєм, потенціал другого волокна буде дещо відрізнятися в часі, оскільки імпульс проходить через два нервові закінчення різної довжини за різний час. Це відображається в мінливості міжпікового інтервалу, тобто час реєстрації другого потенціалу коливається відносно першого, що визначається як "танець" або "тремтіння" потенціалу, значення якого зазвичай становить 5-50 мкс.
Джиттер відображає мінливість часу нервово-м'язової передачі у двох рухових кінцевих пластинках, тому цей метод дозволяє вивчати стабільність нервово-м'язової передачі. При її порушенні будь-якою патологією джиттер збільшується. Його найбільш виражене збільшення спостерігається при синаптичних захворюваннях, насамперед при міастенії.
При значному погіршенні нервово-м'язової передачі виникає стан, коли нервовий імпульс не може збудити одне з двох сусідніх волокон і відбувається так зване блокування імпульсу.
Значне збільшення джиттера та нестабільність окремих компонентів ПМУ також спостерігаються при БАС. Це пояснюється тим, що терміналі та незрілі синапси, що новоутворилися в результаті проростання, функціонують з недостатнім ступенем надійності. У цьому випадку найбільш виражене джиттер та блокування імпульсів спостерігаються у пацієнтів зі швидким прогресуванням процесу.
Макроелектроміографія
Макроелектроміографія дозволяє судити про розміри рухових одиниць у скелетних м'язах. Під час дослідження одночасно використовуються два голчасті електроди: спеціальний макроелектрод, що вводиться глибоко в м'яз так, щоб відвідна бічна поверхня електрода знаходилася в товщі м'яза, та звичайний концентричний електрод, що вводиться під шкіру. Метод макроелектроміографії базується на вивченні потенціалу, що реєструється макроелектродом з великою відвідною поверхнею.
Електродом порівняння служить звичайний концентричний електрод, що вводиться під шкіру на відстані не менше 30 см від основного макроелектрода в зону мінімальної активності досліджуваного м'яза, тобто якомога далі від рухової точки м'яза.
Інший електрод для реєстрації потенціалів окремих м'язових волокон, встановлений у канюлі, реєструє потенціал м'язового волокна досліджуваної МА, що служить тригером для усереднення макропотенціалу. Сигнал з канюлі основного електрода також надходить до усереднювача. Усереднюється 130-200 імпульсів (епоха 80 мс, для аналізу використовується період 60 мс) до появи стабільної ізолінії та стабільного амплітудного макропотенціалу МА. Реєстрація здійснюється за двома каналами: на одному реєструється сигнал від одного м'язового волокна досліджуваної МА, що запускає усереднення, на іншому відтворюється сигнал між основним та опорним електродами.
Основним параметром, який використовується для оцінки макропотенціалу рухової одиниці, є його амплітуда, що вимірюється від піку до піку. Тривалість потенціалу не має значення при використанні цього методу. Можлива оцінка площі макропотенціалів рухової одиниці. У нормі існує широкий діапазон значень її амплітуди, з віком вона дещо збільшується. При нейрогенних захворюваннях амплітуда макропотенціалів рухової одиниці збільшується залежно від ступеня реіннервації в м'язі. При нейрональних захворюваннях вона є найвищою.
На пізніх стадіях захворювання амплітуда макропотенціалів MU зменшується, особливо при значному зниженні м'язової сили, що збігається зі зниженням параметрів MU, зареєстрованих за допомогою стандартної голкової електроміографії.
При міопатіях відзначається зниження амплітуди макропотенціалів рухових одиниць, проте у деяких пацієнтів їх середні значення нормальні, але тим не менш, певна кількість потенціалів зниженої амплітуди все ж відзначається. Жодне з досліджень, що досліджували м'язи пацієнтів з міопатією, не виявило збільшення середньої амплітуди макропотенціалів рухових одиниць.
Метод макроелектроміографії дуже трудомісткий, тому він не набув широкого застосування в рутинній практиці.
Скануюча електроміографія
Метод дозволяє вивчати часовий та просторовий розподіл електричної активності рухової одиниці шляхом сканування, тобто ступінчастого переміщення електрода в області розташування волокон досліджуваної рухової одиниці. Скануюча електроміографія надає інформацію про просторове розташування м'язових волокон по всьому простору рухової одиниці та може опосередковано вказувати на наявність м'язових груп, що утворюються в результаті процесу денервації м'язових волокон та їх повторної реіннервації.
При мінімальному довільному напруженні м'яза електрод, введений у нього для реєстрації окремого м'язового волокна, використовується як тригер, і за допомогою вихідного концентричного голчастого (скануючого) електрода реєструється ПМВ з усіх боків діаметром 50 мм. Метод заснований на повільному поетапному зануренні стандартного голчастого електрода в м'яз, накопиченні інформації про зміну параметрів потенціалу певної МВ та побудові відповідного зображення на екрані монітора. Скануюча електроміографія - це серія осцилограм, розташованих одна під одною, кожна з яких відображає коливання біопотенціалу, зареєстрованого в заданій точці та захопленого вихідною поверхнею концентричного голчастого електрода.
Подальший комп'ютерний аналіз усіх цих MUAP та аналіз їх тривимірного розподілу дає уявлення про електрофізіологічний профіль рухових нейронів.
Під час аналізу даних скануючої електроміографії оцінюється кількість основних піків MUAP, їх зсув у часі появи, тривалість інтервалів між появою окремих фракцій потенціалу даної MU, а також розраховується діаметр зони розподілу волокон у кожній з досліджуваних MU.
При ДРП амплітуда та тривалість, а також площа потенційних коливань на скануючій електроміографії збільшуються. Однак поперечний переріз зони розподілу волокон окремих ДЕ суттєво не змінюється. Кількість фракцій, характерних для даного м'яза, також не змінюється.
Протипоказання до проведення
Протипоказань до голкової електроміографії практично немає. Обмеженням вважається непритомний стан пацієнта, коли він не може довільно напружити м'яз. Однак навіть у цьому випадку можна визначити наявність або відсутність струмового процесу в м'язах (за наявністю або відсутністю спонтанної активності м'язових волокон). Голкову електроміографію слід проводити з обережністю в тих м'язах, які мають виражені гнійні рани, незагойні виразки та глибокі опікові ураження.
Норма
ДЕ є структурним та функціональним елементом скелетного м'яза. Він утворений руховим нейроном, розташованим у передньому розі сірої речовини спинного мозку, його аксон утворює мієлінізоване нервове волокно у складі рухового корінця, та групою м'язових волокон, що утворюють контакт з численними гілками цього аксона, позбавленими мієлінової оболонки – терміналями, за допомогою синапсу.
Кожне м'язове волокно м'яза має власне закінчення, входить до складу лише однієї рухової одиниці та має свій власний синапс. Аксони починають інтенсивно розгалужуватися на рівні кількох сантиметрів перед м'язом, забезпечуючи іннервацію кожного м'язового волокна, що входить до складу цієї рухової одиниці. Руховий нейрон генерує нервовий імпульс, який передається по аксону, посилюється в синапсі та викликає скорочення всіх м'язових волокон, що належать до цієї рухової одиниці. Загальний біоелектричний потенціал, зареєстрований під час такого скорочення м'язових волокон, називається потенціалом рухової одиниці.
Потенціали рухових одиниць
Оцінка стану рухових одиниць скелетних м'язів людини проводиться на основі аналізу параметрів потенціалів, які вони генерують: тривалості, амплітуди та форми. Кожна рухова одиниця утворюється в результаті алгебраїчного додавання потенціалів усіх м'язових волокон, що складають рухову одиницю, яка функціонує як єдине ціле.
Коли хвиля збудження поширюється вздовж м'язових волокон у напрямку електрода, на екрані монітора з'являється трифазний потенціал: перше відхилення позитивне, потім спостерігається швидкий негативний пік, і потенціал завершується третім, знову позитивним відхиленням. Ці фази можуть мати різні амплітуди, тривалості та площі, які залежать від того, як розташована вихідна поверхня електрода відносно центральної частини записаної ДЕ.
Параметри ПМУ відображають розмір ДЕ, кількість, взаємне розташування м'язових волокон та щільність їх розподілу в кожній конкретній ДЕ.
Тривалість нормального потенціалу рухової одиниці
Основним параметром диференціального рівняння в часткових похідних є його тривалість, або довжина, що вимірюється як час у мілісекундах від початку відхилення сигналу від центральної лінії до повного його повернення до неї.
Тривалість ПМУ у здорової людини залежить від м'яза та віку. З віком тривалість ПМУ збільшується. Для створення єдиних критеріїв норми при дослідженні ПМУ розроблені спеціальні таблиці нормальних середніх значень тривалості для різних м'язів людей різного віку. Фрагмент таких таблиць наведено нижче.
Мірою оцінки стану МС у м'язі є середня тривалість 20 різних МСВП, записаних у різних точках досліджуваного м'яза. Середнє значення, отримане під час дослідження, порівнюється з відповідним показником, представленим у таблиці, та розраховується відхилення від норми (у відсотках). Середня тривалість МСВП вважається нормальною, якщо вона знаходиться в межах ±12% від значення, наведеного в таблиці (за кордоном середня тривалість МСВП вважається нормальною, якщо вона знаходиться в межах ±20%).
 [ 14 ], [ 15 ], [ 16 ], [ 17 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ]
Тривалість потенціалів рухових одиниць при патології
Основна закономірність змін тривалості ФДЕ за патологічних станів полягає в тому, що вона збільшується при нейрогенних захворюваннях і зменшується при синаптичній та первинній м'язовій патології.
Для більш ретельної оцінки ступеня зміни ПМУ в м'язах з різними ураженнями периферичного нейромоторного апарату використовується гістограма розподілу ПМУ за тривалістю для кожного м'яза, оскільки їх середнє значення може бути в межах нормальних відхилень при явній м'язовій патології. У нормі гістограма має вигляд нормального розподілу, максимум якого збігається із середньою тривалістю ПМУ для даного м'яза. При будь-якій патології периферичного нейромоторного апарату форма гістограми суттєво змінюється.
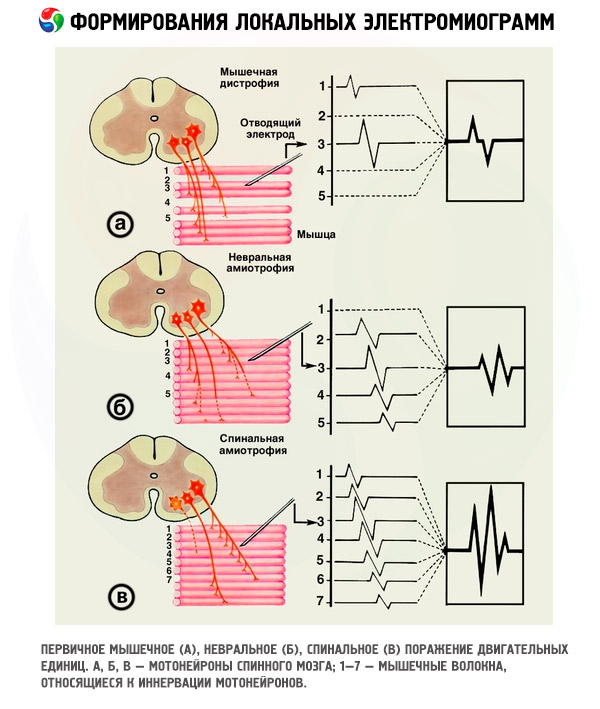
Електроміографічні стадії патологічного процесу
На основі зміни тривалості МУ при захворюваннях рухових нейронів спинного мозку, коли всі зміни, що відбуваються в м'язах, можна простежити за відносно короткий проміжок часу, було виділено шість стадій ЕМГ, які відображають загальні закономірності перебудови МУ в процесі денерваційно-реіннерваційного процесу (ДРП), від самого початку захворювання до майже повної загибелі м'яза.
Усі нейрогенні захворювання характеризуються загибеллю більшої чи меншої кількості рухових нейронів або їх аксонів. Ті, що вижили, іннервують «чужі» м’язові волокна, позбавлені нервового контролю, тим самим збільшуючи їх кількість у своїх МН. На електроміографії цей процес проявляється поступовим збільшенням параметрів потенціалів таких МН. Весь цикл змін гістограми розподілу МН за тривалістю при нейрональних захворюваннях умовно поділяється на п’ять ЕМГ-стадій, що відображають процес компенсаторної іннервації в м’язах. Хоча такий поділ є умовним, він допомагає зрозуміти та простежити всі стадії розвитку ДРП у кожному конкретному м’язі, оскільки кожна стадія відображає певну фазу реіннервації та ступінь її вираженості. Представляти VI стадію у вигляді гістограми недоцільно, оскільки вона відображає кінцеву точку «зворотного» процесу, тобто процес декомпенсації та руйнування МН м’яза.
Серед фахівців нашої країни ці стадії набули широкого поширення в діагностиці різних нервово-м'язових захворювань. Вони включені до комп'ютерної програми вітчизняних електроміографів, що дозволяє автоматично будувати гістограми, що вказують на стадію процесу. Зміна стадії в той чи інший бік під час повторного обстеження пацієнта показує, які подальші перспективи розвитку ДРП.
- I стадія: середня тривалість ПМВП скорочується на 13-20%. Ця стадія відображає саму початкову фазу захворювання, коли денервація вже розпочалася, а процес реіннервації ще не проявляється електроміографічно. Зі складу деяких ПМВП випадають деякі денервовані м'язові волокна, позбавлені імпульсного впливу через патологію або рухового нейрона, або його аксона. Кількість м'язових волокон у таких ПМВП зменшується, що призводить до зменшення тривалості окремих потенціалів. У I стадії з'являється певна кількість вужчих потенціалів, ніж у здоровому м'язі, що спричиняє незначне зменшення середньої тривалості. Гістограма розподілу ПМВП починає зміщуватися вліво, у бік менших значень.
- II стадія: середня тривалість MUAP скорочується на 21% і більше. При DRP ця стадія спостерігається вкрай рідко і лише у випадках, коли з якихось причин реіннервація не відбувається або пригнічується якимось фактором (наприклад, алкоголем, радіацією тощо), тоді як денервація, навпаки, посилюється і відбувається масова загибель м'язових волокон у MUAP. Це призводить до того, що більшість або майже всі MUAP стають коротшими за тривалістю від норми, через що середня тривалість продовжує зменшуватися. Гістограма розподілу MUAP значно зміщується в бік менших значень. Стадії I-II відображають зміни в MUAP, спричинені зменшенням кількості функціонуючих м'язових волокон у них.
- III стадія: середня тривалість ПМВП знаходиться в межах ±20% від норми для даного м'яза. Ця стадія характеризується появою певної кількості потенціалів збільшеної тривалості, в нормі невиявлюваних. Поява цих ПМВП свідчить про початок реіннервації, тобто денервовані м'язові волокна починають включатися до інших ПМВП, завдяки чому параметри їх потенціалів збільшуються. У м'язі одночасно реєструються ПМВП як зниженої, так і нормальної, а також збільшеної тривалості, кількість збільшених ПМВП у м'язі варіюється від одного до кількох. Середня тривалість ПМВП на III стадії може бути нормальною, але зовнішній вигляд гістограми відрізняється від норми. Вона не має форми нормального розподілу, а «сплющується», розтягується і починає зміщуватися праворуч, у бік більших значень. Запропоновано розділити III стадію на дві підгрупи - IIIA та IIIB. Вони відрізняються лише тим, що на стадії IIIA середня тривалість MUAP зменшується на 1-20%, а на стадії IIIB вона або повністю збігається із середнім значенням норми, або збільшується на 1-20%. На стадії IIIB реєструється дещо більша кількість MUAP збільшеної тривалості, ніж на стадії IIIA. Практика показала, що такий поділ третьої стадії на дві підгрупи не має великого значення. Фактично, стадія III означає просто появу перших ЕМГ-ознак реіннервації в м'язі.
- IV стадія: середня тривалість MUAP збільшується на 21-40%. Ця стадія характеризується збільшенням середньої тривалості MUAP через появу поряд з нормальними MUAP великої кількості потенціалів збільшеної тривалості. MUAP зменшеної тривалості на цій стадії реєструються вкрай рідко. Гістограма зміщена праворуч, у бік більших значень, її форма різна та залежить від співвідношення MUAP нормальної та збільшеної тривалості.
- V стадія: середня тривалість MUAP збільшена на 41% і більше. Ця стадія характеризується наявністю переважно великих і «гігантських» MUAP, тоді як MUAP нормальної тривалості практично відсутні. Гістограма значно зміщена праворуч, розтягнута та, як правило, відкрита. Ця стадія відображає максимальний обсяг реіннервації в м'язі, а також її ефективність: чим більше гігантських MUAP, тим ефективніша реіннервація.
- VI стадія: середня тривалість ПМП знаходиться в межах норми або скорочена більш ніж на 12%. Ця стадія характеризується наявністю ПМП (потенціалів деградуючих ПМП), які змінені за формою. Їхні параметри формально можуть бути нормальними або зниженими, але форма ПМП змінена: потенціали не мають різких піків, розтягнуті, округлі, час наростання потенціалу різко збільшений. Ця стадія спостерігається на останній стадії декомпенсації ДРП, коли більшість рухових нейронів спинного мозку вже загинули, а решта інтенсивно гинуть. Декомпенсація процесу починається з моменту, коли процес денервації посилюється, а джерел іннервації стає все менше. На ЕМГ стадія декомпенсації характеризується такими ознаками: параметри ПМП починають знижуватися, гігантські ПМП поступово зникають, інтенсивність ПФ різко зростає, з'являються гігантські ПОВ, що свідчить про загибель багатьох прилеглих м'язових волокон. Ці ознаки свідчать про те, що в цьому м'язі рухові нейрони вичерпали свої проросткові можливості внаслідок функціональної недостатності та більше не здатні повноцінно контролювати свої волокна. В результаті цього кількість м'язових волокон у руховій одиниці прогресивно зменшується, порушуються механізми проведення імпульсів, потенціали таких рухових одиниць заокруглюються, зменшується їх амплітуда та зменшується їх тривалість. Побудова гістограми на цьому етапі процесу недоцільна, оскільки вона, як і середня тривалість ПМО, вже не відображає справжнього стану м'яза. Основною ознакою VI стадії є зміна форми всіх ПМО.
Стадії ЕМГ використовуються не лише для нейрогенних захворювань, а й для різних первинних м'язових захворювань, для характеристики глибини м'язової патології. У цьому випадку стадія ЕМГ відображає не ДРП, а тяжкість патології та називається «ЕМГ-стадією патологічного процесу». При первинних м'язових дистрофіях можуть з'являтися різко поліфазні ПМУ із супутниками, що збільшують їх тривалість, що значно збільшує її середнє значення, що відповідає III або навіть IV ЕМГ-стадії патологічного процесу.
Діагностичне значення стадій ЕМГ
- При нейрональних захворюваннях у одного пацієнта в різних м'язах часто виявляються різні стадії ЕМГ – стадії від III до VI виявляються дуже рідко – на самому початку захворювання, і лише в окремих м'язах.
- При аксональних та демієлінізуючих захворюваннях найчастіше виявляються III та IV стадії, а I та II – рідше. V стадія виявляється, коли значна кількість аксонів гине в окремих, найбільш уражених м’язах.
- При первинних м'язових захворюваннях спостерігається втрата м'язових волокон зі складу ММ через якусь м'язову патологію: зменшення діаметра м'язових волокон, їх розщеплення, фрагментація або інше пошкодження, що зменшує кількість м'язових волокон у ММ або зменшує об'єм м'яза. Все це призводить до зменшення (скорочення) тривалості ПММ. Тому при більшості первинних м'язових захворювань та міастенії виявляються I та II стадії, при поліміозиті - спочатку лише I та I, а після одужанні - III та навіть IV стадії.
Амплітуда потенціалу рухової одиниці
Амплітуда є допоміжним, але дуже важливим параметром при аналізі MUAP. Вона вимірюється «від піку до піку», тобто від найнижчої точки позитивного до найвищої точки негативного піку. При реєстрації MUAP на екрані їх амплітуда визначається автоматично. Визначається як середня, так і максимальна амплітуда MUAP, виявленого в досліджуваному м'язі.
Середні значення амплітуди MUAP у проксимальних м'язах здорових людей у більшості випадків становлять 500-600 мкВ, у дистальних м'язах - 600-800 мкВ, при цьому максимальна амплітуда не перевищує 1500-1700 мкВ. Ці показники дуже умовні та можуть дещо змінюватися. У дітей віком 8-12 років середня амплітуда MUAP, як правило, знаходиться в межах 300-400 мкВ, а максимальна не перевищує 800 мкВ; у дітей старшого віку ці показники становлять 500 та 1000 мкВ відповідно. У мімічних м'язах амплітуда MUAP значно нижча.
У спортсменів у тренованих м'язах реєструється підвищена амплітуда середньої амплітуди середньої амплітуди середньої амплітуди середньої амплітуди середньої амплітуди у м'язах здорових осіб, що займаються спортом, не можна вважати патологією, оскільки воно виникає в результаті перебудови середньої амплітуди середньої амплітуди внаслідок тривалого навантаження на м'язи.
При всіх нейрогенних захворюваннях амплітуда ПМУ, як правило, збільшується відповідно до збільшення тривалості: чим довша тривалість потенціалу, тим вища його амплітуда.
Найбільш значне збільшення амплітуди MUAP спостерігається при нейрональних захворюваннях, таких як спінальна аміотрофія та наслідки поліомієліту. Це служить додатковим критерієм для діагностики нейрогенної природи патології в м'язах. Збільшення амплітуди MUAP зумовлене реорганізацією MU в м'язі, збільшенням кількості м'язових волокон у зоні підведення електрода, синхронізацією їхньої активності та збільшенням діаметра м'язових волокон.
Збільшення як середньої, так і максимальної амплітуди MUAP іноді спостерігається при деяких первинних м'язових захворюваннях, таких як поліміозит, первинна м'язова дистрофія, дистрофічна міотонія тощо.
Хвиля потенціалу рухового блоку
Форма ПДЕ залежить від структури ДЕ, ступеня синхронізації потенціалів її м'язових волокон, положення електрода відносно м'язових волокон аналізованої ДЕ та зон їх іннервації. Форма потенціалу не має діагностичного значення.
У клінічній практиці форма MUAP аналізується з точки зору кількості фаз та/або поворотів потенціалу. Кожне позитивно-негативне відхилення потенціалу, яке досягає ізолінії та перетинає її, називається фазою, а позитивно-негативне відхилення потенціалу, яке не досягає ізолінії, називається поворотом.
Потенціал вважається поліфазним, якщо він має п'ять або більше фаз і перетинає осьову лінію щонайменше чотири рази. Потенціал може мати додаткові витки, які не перетинають осьову лінію. Витки можуть бути як у негативній, так і в додатній частинах потенціалу.
У м'язах здорових людей MUAP зазвичай представлені трифазними потенціальними коливаннями, проте під час реєстрації MUAP в зоні кінцевої пластинки він може мати дві фази, втрачаючи свою початкову позитивну частину.
У нормі кількість поліфазних MUAP не перевищує 5-15%. Збільшення кількості поліфазних MUAP вважається ознакою порушення структури MU через наявність якогось патологічного процесу. Поліфазні та псевдополіфазні MUAP реєструються як при нейрональних, так і при аксональних захворюваннях, а також при первинних м'язових захворюваннях.
 [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Спонтанна активність
За нормальних умов, коли електрод нерухомий у розслабленому м'язі здорової людини, електричної активності не виникає. При патології з'являється спонтанна активність м'язових волокон або ДЕ. Спонтанна активність не залежить від волі пацієнта, він не може її зупинити або викликати довільно.
Спонтанна активність м'язових волокон
Спонтанна активність м'язових волокон включає потенціали фібриляції (ФФ) та позитивні гострі хвилі (ПГХ). ФФ та ГГХ реєструються виключно за патологічних умов, коли в м'яз введено концентричний голчастий електрод. ФФ – потенціал одного м'язового волокна, ГГХ – повільне коливання, що виникає після швидкого позитивного відхилення, без різкого негативного піку. ГГХ відображає участь як одного, так і кількох сусідніх волокон.
Вивчення спонтанної активності м'язових волокон в умовах клінічного обстеження пацієнта є найзручнішим електрофізіологічним методом, що дозволяє судити про ступінь повноти та стабільності нервових впливів на м'язові волокна скелетного м'яза при його патології.
Спонтанна активність м'язових волокон може виникати при будь-якій патології периферичного нейромоторного апарату. При нейрогенних захворюваннях, а також при патології синапсів (міастенія та міастенічні синдроми) спонтанна активність м'язових волокон відображає процес їх денервації. При більшості первинних захворювань м'язів спонтанна активність м'язових волокон відображає певне пошкодження м'язових волокон (їх розщеплення, фрагментацію тощо), а також їх патологію, спричинену запальним процесом (при запальних міопатіях - поліміозиті, дерматоміозиті). В обох випадках ПФ та ПОВ вказують на наявність процесу, що триває в м'язі; у нормі вони ніколи не реєструються.
- Тривалість ПФ становить 1-5 мс (діагностичного значення не має), а амплітуда коливається в дуже широких межах (в середньому 118±114 мкВ). Іноді виявляються також високоамплітудні (до 2000 мкВ) ПФ, зазвичай у пацієнтів із хронічними захворюваннями. Терміни появи ПФ залежать від місця ураження нерва. У більшості випадків вони виникають через 7-20 днів після денервації.
- Якщо з якихось причин реіннервація денервованого м'язового волокна не відбувається, воно з часом гине, генеруючи ПОВ, які за допомогою ЕМГ розглядаються як ознака загибелі денервованого м'язового волокна, яке не отримало втраченої ним раніше іннервації. За кількістю ПФ та ПОВ, зареєстрованих у кожному м'язі, можна опосередковано судити про ступінь та глибину його денервації або об'єм загиблих м'язових волокон. Тривалість ПОВ становить від 1,5 до 70 мс (у більшості випадків до 10 мс). Так звані гігантські ПОВ тривалістю понад 20 мс виявляються при тривалій денервації великої кількості сусідніх м'язових волокон, а також при поліміозиті. Амплітуда ПОВ зазвичай коливається між 10 та 1800 мкВ. ПОВ великої амплітуди та тривалості частіше виявляються на пізніх стадіях денервації («гігантські» ПОВ). ПОВ вперше реєструються через 16-30 днів після першої появи ПФ; вони можуть зберігатися в м'язі протягом кількох років після денервації. Як правило, ПОВ виявляються пізніше у пацієнтів із запальними ураженнями периферичних нервів, ніж у пацієнтів з травматичними ураженнями.
ПФ та ПОВ найшвидше реагують на початок терапії: якщо вона ефективна, тяжкість ПФ та ПОВ зменшується через 2 тижні. Навпаки, якщо лікування неефективне або недостатньо ефективне, їх тяжкість зростає, що дозволяє використовувати аналіз ПФ та ПОВ як показник ефективності застосовуваних препаратів.
Міотонічні та псевдоміотонічні розряди
Міотонічні та псевдоміотонічні розряди, або високочастотні розряди, також відносяться до спонтанної активності м'язових волокон. Міотонічні та псевдоміотонічні розряди відрізняються низкою ознак, головною з яких є висока повторюваність елементів, що складають розряд, тобто висока частота потенціалів у розряді. Термін «псевдоміотонічний розряд» все частіше замінюється терміном «високочастотний розряд».
- Міотонічні розряди – це явище, яке виявляється у пацієнтів з різними формами міотонії. При прослуховуванні він нагадує звук «пікіруючого бомбардувальника». На екрані монітора ці розряди виглядають як повторювані потенціали поступово зменшуваної амплітуди, з прогресивно зростаючими інтервалами (що спричиняє зниження висоти звуку). Міотонічні розряди іноді спостерігаються при деяких формах ендокринної патології (наприклад, гіпотиреоз). Міотонічні розряди виникають або спонтанно, або після легкого скорочення чи механічного подразнення м’яза введеним у нього голчастим електродом, або простим постукуванням по м’язу.
- Псевдоміотонічні розряди (високочастотні розряди) реєструються при деяких нервово-м'язових захворюваннях, як пов'язаних, так і не пов'язаних з денервацією м'язових волокон. Їх вважають наслідком ефаптичної передачі збудження зі зниженням ізоляційних властивостей мембрани м'язових волокон, що створює передумову для поширення збудження з одного волокна на сусіднє: пейсмейкер одного з волокон задає ритм імпульсів, який нав'язується сусіднім волокнам, що зумовлює унікальну форму комплексів. Розряди починаються та припиняються раптово. Їхня основна відмінність від міотонічних розрядів полягає у відсутності падіння амплітуди компонентів. Псевдоміотонічні розряди спостерігаються при різних формах міопатії, поліміозиті, денерваційних синдромах (на пізніх стадіях реіннервації), спінальних та нейронних аміотрофіях (хвороба Шарко-Марі-Тута), ендокринній патології, травмах або стисканні нерва та деяких інших захворюваннях.
Спонтанна активність рухових одиниць
Спонтанна активність рухової одиниці представлена фасцикуляційними потенціалами. Фасцикуляції – це спонтанні скорочення всієї рухової одиниці, що відбуваються в повністю розслабленому м'язі. Їх виникнення пов'язане із захворюваннями рухового нейрона, його перевантаженням м'язовими волокнами, подразненням будь-якого з його відділів, функціональною та морфологічною перебудовою.
Поява множинних фасцикуляційних потенціалів у м'язах вважається однією з основних ознак пошкодження рухових нейронів спинного мозку. Винятком є «доброякісні» фасцикуляційні потенціали, які іноді виявляються у пацієнтів, які скаржаться на постійне посмикування в м'язах, але не відзначають м'язової слабкості чи інших симптомів.
Поодинокі фасцикуляційні потенціали також можуть бути виявлені при нейрогенних і навіть первинних м'язових захворюваннях, таких як міотонія, поліміозит, ендокринні, метаболічні та мітохондріальні міопатії.
Описано фасцикуляційні потенціали, що виникають у висококваліфікованих спортсменів після виснажливих фізичних навантажень. Вони також можуть виникати у здорових, але легко збудливих людей, у пацієнтів з тунельними синдромами, полінейропатіями та у людей похилого віку. Однак, на відміну від захворювань рухових нейронів, їх кількість у м'язі дуже мала, а параметри зазвичай нормальні.
Параметри фасцикуляційних потенціалів (амплітуда та тривалість) відповідають параметрам MUAP, зареєстрованим у даному м'язі, і можуть змінюватися паралельно зі змінами MUAP під час розвитку захворювання.
Голкова електроміографія в діагностиці захворювань рухових нейронів спинного мозку та периферичних нервів
Будь-яка нейрогенна патологія супроводжується ДРП, тяжкість якої залежить від ступеня пошкодження джерел іннервації та від рівня периферичного нейромоторного апарату – нейронального чи аксонального – на якому відбулося пошкодження. В обох випадках втрачена функція відновлюється за рахунок нервових волокон, що збереглися, і останні починають інтенсивно гілкуватися, утворюючи численні пагони, спрямовані до денервованих м'язових волокон. Це розгалуження отримало в літературі назву «спроутинг».
Існує два основних типи проростання – колатеральне та термінальне. Колатеральне проростання – це розгалуження аксонів у ділянці вузлів Ранв'є, термінальне проростання – це розгалуження кінцевої, немієлінізованої ділянки аксона. Показано, що характер проростання залежить від природи фактора, який спричинив порушення нервового контролю. Наприклад, при ботулотоксичній інтоксикації розгалуження відбувається виключно в термінальній зоні, а при хірургічній денервації відбувається як термінальне, так і колатеральне проростання.
В електроміографії ці стани MU на різних етапах процесу реіннервації характеризуються появою MUAP підвищеної амплітуди та тривалості. Винятком є самі початкові стадії бульбарної форми БАС, при яких параметри MUAP знаходяться в межах нормальних коливань протягом кількох місяців.
Електроміографічні критерії захворювань рухових нейронів спинного мозку
- Наявність виражених фасцикуляційних потенціалів (основний критерій пошкодження рухових нейронів спинного мозку).
- Збільшення параметрів ПДЕ та їх поліфазність, що відображає вираженість процесу реіннервації.
- Поява спонтанної активності м'язових волокон у м'язах - PF та POV, що свідчить про наявність триваючого процесу денервації.
Фасцикуляційні потенціали є обов'язковою електрофізіологічною ознакою пошкодження рухових нейронів спинного мозку. Вони виявляються вже на самих ранніх стадіях патологічного процесу, ще до появи ознак денервації.
Оскільки нейрональні захворювання передбачають постійний процес денервації та реіннервації, коли велика кількість рухових нейронів гине, а відповідна кількість рухових нейронів руйнується одночасно, розміри рухових нейронів збільшуються, їхня тривалість та амплітуда збільшуються. Ступінь збільшення залежить від тривалості та стадії захворювання.
Тяжкість ПФ та ПОВ залежить від тяжкості патологічного процесу та ступеня денервації м'язів. При швидкопрогресуючих захворюваннях (наприклад, БАС) ПФ та ПОВ виявляються в більшості м'язів, при повільно прогресуючих захворюваннях (деякі форми спінальних аміотрофій) - лише в половині м'язів, а при постполіомієлітному синдромі - менш ніж у третині.
Електроміографічні критерії захворювань аксонів периферичних нервів
Голкова електроміографія в діагностиці захворювань периферичних нервів є додатковим, але необхідним методом обстеження, що визначає ступінь пошкодження м'яза, іннервованого ураженим нервом. Дослідження дозволяє уточнити наявність ознак денервації (ДД), ступінь втрати м'язових волокон у м'язі (загальна кількість МДВ та наявність гігантських МДВ), вираженість реіннервації та її ефективність (ступінь збільшення параметрів МДВ, максимальна амплітуда МДВ у м'язі).
Основні електроміографічні ознаки аксонального відростка:
- збільшення середнього значення амплітуди диференціального рівняння в похідних;
- наявність ПФ та ПОВ (при поточній денервації);
- збільшення тривалості ПДЕ (середнє значення може бути в межах норми, тобто ±12%);
- поліфазія ПДЕ;
- поодинокі фасцикуляційні потенціали (не в кожному м'язі).
У разі пошкодження аксонів периферичних нервів (різні полінейропатії) також виникає ДРП, але її вираженість значно менша, ніж при нейрональних захворюваннях. Отже, ПНП підвищені в значно меншій мірі. Проте, основне правило зміни ПНП при нейрогенних захворюваннях стосується і пошкодження аксонів рухових нервів (тобто ступінь збільшення параметрів ПНП та їх поліфазність залежать від ступеня пошкодження нерва та вираженості реіннервації). Винятком є патологічні стани, що супроводжуються швидкою загибеллю аксонів рухових нервів внаслідок травми (або якогось іншого патологічного стану, що призводить до загибелі великої кількості аксонів). У цьому випадку виникають такі ж гігантські ПНП (з амплітудою понад 5000 мкВ), як і при нейрональних захворюваннях. Такі ПНП спостерігаються при тривалих формах аксональної патології, ХВДП, нейронних аміотрофіях.
Якщо при аксональних полінейропатіях амплітуда MUAP збільшується насамперед, то в демієлінізуючому процесі з погіршенням функціонального стану м'яза (зниженням його сили) середні значення тривалості MUAP поступово збільшуються; значно частіше, ніж в аксональному процесі, виявляються поліфазні MUAP та фасцикуляційні потенціали і рідше - PF та POV.
 [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ]
[ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ]
Голкова електроміографія в діагностиці синаптичних та первинних м'язових захворювань
Синаптичні та первинні м'язові захворювання зазвичай мають зменшення середньої тривалості середньої перерви у перехідному положенні (MUAP). Ступінь зменшення тривалості MUAP корелює зі зниженням сили. У деяких випадках параметри MUAP знаходяться в межах норми, а при постменструальному дисфункції (PMD) вони навіть можуть бути підвищені.

